Bahan aktif: Ramipril
TRIATEC tablet 1,25 mg
TRIATEC tablet 2,5 mg
TRIATEC tablet 5 mg
TRIATEC tablet 10 mg
Indikasi Mengapa Triatec digunakan? Untuk apa?
TRITACE mengandung obat yang disebut ramipril yang termasuk dalam kelompok obat yang disebut ACE inhibitor (Angiotensin Converting Enzyme Inhibitors).
TRIATEC bertindak:
- Dengan mengurangi produksi zat-zat yang dapat menyebabkan tekanan darah naik
- Relaksasi dan pelebaran pembuluh darah Anda
- Memudahkan jantung Anda untuk memompa darah ke seluruh tubuh Anda.
TRIATEC dapat digunakan:
- Untuk mengobati tekanan darah tinggi (hipertensi)
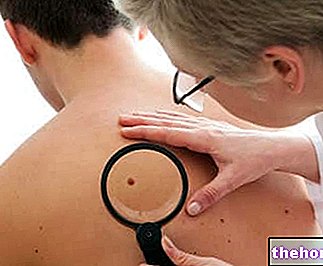
- Untuk mengurangi risiko serangan jantung atau stroke
- Untuk mengurangi risiko atau menunda memburuknya masalah ginjal (apakah Anda menderita diabetes atau tidak)
- Untuk mengobati jantung Anda ketika tidak dapat memompa cukup darah ke seluruh tubuh (gagal jantung)
- Sebagai pengobatan setelah serangan jantung (infark miokard) bila dikaitkan dengan gagal jantung.
Kontraindikasi Ketika Triatec tidak boleh digunakan
Jangan mengambil TRITACE:
- Jika Anda alergi (hipersensitif) terhadap ramipril, obat ACE inhibitor lain atau salah satu bahan lain dari TRITACE yang tercantum di bagian 6. Tanda-tanda reaksi alergi mungkin ruam kulit, kesulitan menelan atau bernapas, pembengkakan bibir, wajah, di tenggorokan atau lidah
- Jika Anda pernah mengalami reaksi alergi parah yang disebut 'angioedema'. Tanda-tandanya antara lain gatal-gatal, ruam (gatal-gatal), bintik-bintik merah pada tangan, kaki dan tenggorokan, pembengkakan tenggorokan dan lidah, pembengkakan di sekitar mata dan bibir, kesulitan bernapas dan menelan.
- Jika Anda menjalani dialisis atau melakukan beberapa jenis penyaringan darah lainnya. Tergantung pada mesin yang digunakan, TRIATEC mungkin tidak cocok untuk Anda
- Jika Anda memiliki masalah ginjal karena suplai darah yang tidak mencukupi ke ginjal (stenosis arteri ginjal).
- Selama 6 bulan terakhir kehamilan (lihat bagian di bawah "Kehamilan dan menyusui")
- Jika tekanan darah Anda terlalu rendah atau tidak stabil. Dokter Anda perlu melakukan penilaian ini
- Jika Anda menderita diabetes atau gangguan fungsi ginjal dan Anda sedang dirawat dengan obat penurun tekanan darah yang mengandung aliskiren.
Jangan mengambil TRITACE jika salah satu dari kondisi di atas berlaku. Jika Anda tidak yakin, tanyakan kepada dokter Anda sebelum mengambil TRITACE.
Kewaspadaan penggunaan Apa yang perlu Anda ketahui sebelum menggunakan Triatec
Periksa dengan dokter atau apoteker Anda sebelum mengambil TRITACE:
- Jika Anda memiliki masalah jantung, hati atau ginjal
- Jika Anda kehilangan banyak garam atau cairan tubuh (karena tidak sehat seperti muntah, diare, keringat berlebih, atau mengikuti diet rendah garam, atau karena mengonsumsi diuretik dalam jangka waktu lama atau menjalani cuci darah)
- Jika Anda akan menjalani pengobatan untuk mengurangi alergi terhadap sengatan lebah atau tawon (desensitization)
- Jika Anda akan menjalani anestesi. Ini mungkin diberikan untuk operasi atau perawatan gigi. Anda mungkin perlu berhenti minum TRITACE sehari sebelumnya; mintalah nasihat dokter Anda
- Jika Anda memiliki jumlah kalium yang tinggi dalam darah Anda (ditunjukkan dalam tes darah)
- Anda sedang mengonsumsi obat-obatan atau berada dalam kondisi di mana kadar natrium darah Anda mungkin turun. Dokter Anda mungkin memesan tes darah secara berkala, terutama untuk memeriksa kadar natrium darah Anda, terutama jika Anda berusia lanjut
- Jika Anda memiliki penyakit kolagen vaskular seperti skleroderma atau lupus eritematosus sistemik.
- Anda harus memberi tahu dokter Anda jika Anda merasa (atau mungkin) hamil. TRIATEC tidak dianjurkan dalam 3 bulan pertama kehamilan dan dapat menyebabkan bahaya serius pada bayi setelah 3 bulan kehamilan (lihat bagian di bawah "Kehamilan dan menyusui")
- Jika Anda sedang mengonsumsi obat-obatan berikut yang digunakan untuk mengobati tekanan darah tinggi: - "antagonis reseptor angiotensin II" (AIIRA) (juga dikenal sebagai sartans - misalnya valsartan, telmisartan, irbesartan), terutama jika Anda memiliki masalah ginjal yang berkaitan dengan diabetes - aliskiren "
Dokter Anda mungkin memeriksa fungsi ginjal, tekanan darah, dan jumlah elektrolit (seperti kalium) dalam darah Anda secara berkala. Lihat juga informasi di bawah judul "Jangan mengambil TRITACE".
Anak-anak
Penggunaan TRITACE tidak dianjurkan pada anak-anak dan remaja di bawah usia 18 tahun karena keamanan dan kemanjuran TRITACE pada anak-anak belum ditetapkan.
Jika salah satu di atas berlaku untuk Anda (atau Anda tidak yakin), tanyakan kepada dokter Anda sebelum mengambil TRITACE.
Interaksi Obat atau makanan mana yang dapat mengubah efek Triatec
Beri tahu dokter atau apoteker Anda jika Anda sedang atau baru saja mengonsumsi obat lain, termasuk obat yang diperoleh tanpa resep (termasuk obat herbal). Ini karena TRITACE dapat mempengaruhi cara kerja beberapa obat lain.
Juga beberapa obat dapat mempengaruhi cara kerja TRITACE.
Beri tahu dokter Anda jika Anda sedang mengonsumsi obat-obatan berikut. Obat-obatan ini dapat mengganggu TRITACE dengan mengubah aksinya:
- Obat-obatan yang digunakan untuk menghilangkan rasa sakit dan peradangan (misalnya Obat Antiinflamasi Non Steroid (NSAID) seperti ibuprofen, indometasin, aspirin)
- Obat-obatan yang digunakan untuk mengobati tekanan darah rendah, syok, gagal jantung, asma atau alergi seperti efedrin, noradrenalin atau adrenalin. Dokter Anda perlu memeriksa tekanan darah Anda.
Beri tahu dokter Anda jika Anda sedang mengonsumsi obat-obatan berikut. Obat-obatan ini, bila diminum dengan TRITACE, dapat meningkatkan kemungkinan mengalami efek samping:
- Obat-obatan yang digunakan untuk menghilangkan rasa sakit dan peradangan (misalnya Obat Antiinflamasi Non Steroid (NSAID) seperti ibuprofen, indometasin, aspirin)
- Obat-obatan untuk mengobati kanker (kemoterapi)
- Obat-obatan untuk menghindari penolakan organ setelah transplantasi seperti siklosporin
- Diuretik seperti furosemide
- Obat-obatan yang dapat meningkatkan jumlah kalium dalam darah seperti spironolactone, triamterene, amiloride, garam kalium dan heparin (digunakan untuk mengencerkan darah)
- Obat steroid untuk pengobatan peradangan seperti prednisolon
- Allopurinol (digunakan untuk menurunkan kadar asam urat dalam darah)
- Procainamide (untuk masalah detak jantung)
- Berhati-hatilah dengan TRIATEC ").
Beri tahu dokter Anda jika Anda sedang mengonsumsi obat-obatan berikut. Mekanisme kerja obat-obatan ini dapat dipengaruhi oleh TRITACE:
- Obat-obatan untuk diabetes seperti hipoglikemik oral dan insulin.TRITACE dapat menurunkan jumlah gula dalam darah Anda.Periksa kadar gula darah Anda dengan hati-hati saat menggunakan TRITACE.
- Lithium (untuk masalah kejiwaan). TRITACE dapat meningkatkan jumlah lithium dalam darah. Tingkat lithium dalam darah Anda harus diperiksa dengan cermat oleh dokter Anda.
Jika salah satu di atas berlaku untuk Anda (atau Anda tidak yakin), tanyakan kepada dokter Anda sebelum mengambil TRITACE.
Mengambil TRITACE dengan makanan dan alkohol
- Minum minuman beralkohol bersama dengan TRITACE dapat menyebabkan Anda merasa pusing atau pusing. Jika Anda ingin mengetahui berapa banyak alkohol yang harus diminum saat Anda menggunakan TRITACE, diskusikan hal ini dengan dokter Anda, karena obat yang digunakan untuk menurunkan tekanan darah dan alkohol mungkin memiliki reseptor angiotensin II (AIIRA) atau aliskiren (lihat juga informasi di bawah "Jangan ambil TRITACE" dan "efek aditif.
- TRIATEC dapat dikonsumsi bersama atau setelah makan.
Peringatan Penting untuk diketahui bahwa:
Kehamilan
Anda harus memberi tahu dokter Anda jika Anda merasa (atau mungkin) hamil.
Anda tidak boleh mengonsumsi TRITACE dalam 12 minggu pertama kehamilan dan Anda tidak boleh meminumnya sama sekali setelah minggu ke-13 karena penggunaannya selama kehamilan dapat berbahaya bagi bayi. Jika Anda hamil saat menggunakan Triatec, harap segera beri tahu dokter Anda.
Sebelum merencanakan kehamilan, peralihan ke obat lain yang lebih cocok harus dilakukan.
Waktunya memberi makan
Anda tidak harus mengambil TRITACE jika Anda sedang menyusui. Tanyakan kepada dokter atau apoteker Anda sebelum minum obat apa pun.
Mengemudi dan menggunakan mesin
Anda mungkin merasa pusing saat menggunakan TRITACE. Ini lebih mungkin terjadi ketika Anda baru saja mulai menggunakan TRITACE atau baru saja meningkatkan dosis Anda. Jika ini terjadi, jangan mengemudi atau menggunakan alat atau mesin apa pun.
Dosis, Cara dan Waktu Pemberian Cara Pemakaian Triatec: Posology
Selalu gunakan TRITACE persis seperti yang dikatakan dokter Anda. Anda harus mencari nasihat dari dokter atau apoteker Anda jika Anda tidak yakin.
Minum obat ini
- Minum obat ini melalui mulut pada waktu yang sama setiap hari
- Telan tablet utuh dengan cairan.
- Jangan merusak tablet atau mengunyahnya.
Berapa banyak yang harus Anda ambil?
Pengobatan tekanan darah tinggi
- Dosis awal yang biasa adalah 1,25 mg atau 2,5 mg sekali sehari.
- Dokter Anda akan menyesuaikan jumlah yang Anda ambil sampai tekanan darah Anda terkendali.
- Dosis harian maksimum adalah 10 mg.
- Jika Anda sudah menggunakan diuretik, dokter Anda mungkin menghentikan atau mengurangi jumlahnya sebelum memulai pengobatan dengan TRITACE.
Untuk mengurangi risiko serangan jantung atau stroke
- Dosis awal adalah 2,5 mg sekali sehari.
- Dokter Anda mungkin memutuskan untuk meningkatkan dosis yang Anda ambil
- Dosis biasa adalah 10 mg sekali sehari.
Perawatan untuk mengurangi atau mencegah memburuknya masalah ginjal
- Anda mungkin diberikan dosis awal 1,25 mg atau 2,5 mg sekali sehari
- Dokter Anda akan menyesuaikan jumlah yang Anda pakai.
- Dosis biasa adalah 5 mg atau 10 mg sekali sehari.
Pengobatan gagal jantung
- Dosis awal yang biasa adalah 1,25 mg sekali sehari.
- Dokter Anda akan menyesuaikan jumlah yang Anda ambil.
- Dosis maksimum adalah 10 mg per hari. Lebih disukai untuk membagi dosis menjadi dua administrasi harian.
Perawatan setelah serangan jantung
- Dosis awal yang biasa adalah 1,25 mg sekali sehari hingga 2,5 mg dua kali sehari.
- Dokter Anda akan menyesuaikan jumlah yang Anda ambil.
- Dosis biasa adalah 10 mg per hari. Lebih disukai untuk membagi dosis menjadi dua administrasi harian.
Warga senior
Dokter Anda akan mengurangi dosis awal dan menyesuaikan pengobatan Anda lebih lambat.
Overdosis Apa yang harus dilakukan jika Anda mengonsumsi terlalu banyak Triatec
Jika Anda mengambil TRITACE lebih dari yang seharusnya
Beri tahu dokter Anda atau pergi ke ruang gawat darurat rumah sakit terdekat. Jangan mengemudi ke rumah sakit, mintalah seseorang menemani Anda atau panggil ambulans. Bawalah kotak obat bersama Anda. Ini karena dokter Anda perlu tahu apa yang Anda sewa .
Jika Anda lupa mengambil TRITACE
- Jika Anda melewatkan satu dosis, minumlah dosis normal Anda pada waktunya.
- Jangan mengambil dosis ganda untuk mengganti tablet yang terlupakan.
Jika Anda memiliki pertanyaan lebih lanjut tentang penggunaan obat ini, tanyakan kepada dokter atau apoteker Anda.
Efek Samping Apa efek samping dari Triatec
Seperti semua obat-obatan, TRITACE dapat menyebabkan efek samping, meskipun tidak semua orang mendapatkannya.
Hentikan penggunaan TRITACE dan segera temui dokter Anda jika Anda melihat adanya efek samping yang serius - Anda mungkin memerlukan perawatan medis segera:
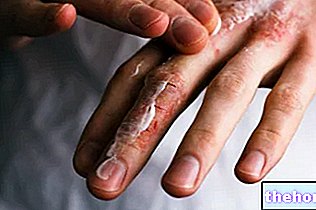
- Pembengkakan pada wajah, bibir atau tenggorokan yang membuat sulit menelan atau bernapas, serta gatal atau ruam. Ini bisa menjadi tanda reaksi alergi parah terhadap TRITACE.
- Reaksi kulit yang parah termasuk ruam, sariawan, memburuknya kondisi kulit yang sudah ada sebelumnya, kemerahan, lepuh dan pengelupasan kulit (seperti Sindrom Stevens-Johnson, nekrolisis epidermal toksik atau eritema multiforme).
Beritahu dokter Anda segera jika Anda mengalami:
- Detak jantung lebih cepat, detak jantung tidak teratur atau menguat (palpitasi), nyeri dada, sesak di dada, atau masalah yang lebih serius termasuk serangan jantung dan stroke
- Sesak napas atau batuk. Ini bisa menjadi tanda masalah paru-paru
- Lebih mudah memar, berdarah lebih lama dari biasanya, tanda-tanda perdarahan (misalnya gusi berdarah) bintik-bintik ungu pada kulit atau infeksi yang lebih mudah, iritasi tenggorokan dan demam, merasa lelah, lemah, pusing atau kulit pucat. Ini bisa menjadi tanda masalah darah atau sumsum tulang
- Sakit perut parah yang bisa meluas ke punggung. Ini bisa menjadi tanda pankreatitis (radang pankreas)
- Demam, menggigil, lelah, kehilangan nafsu makan, sakit perut, merasa mual, kulit atau mata menguning (jaundice). Ini mungkin merupakan tanda-tanda masalah hati seperti hepatitis (radang hati) atau kerusakan hati. .
Efek samping lainnya termasuk:
Beri tahu dokter Anda jika salah satu kondisi yang dijelaskan di bawah ini menjadi parah atau bertahan lebih dari beberapa hari:
Umum (mempengaruhi kurang dari 1 pasien dalam setiap 10 pasien yang menjalani terapi)
- Sakit kepala atau perasaan lelah
- Merasa pusing. Ini lebih mungkin terjadi ketika terapi TRITACE baru saja dimulai atau dosisnya baru saja ditingkatkan
- Kelemahan, hipotensi (tekanan darah rendah yang luar biasa), terutama saat berdiri atau bangun dengan cepat
- Batuk kering yang mengiritasi, radang sinus (sinusitis) atau bronkitis, sesak napas
- Sakit di perut atau usus, diare, gangguan pencernaan, merasa tidak enak badan atau tidak sehat
- Ruam kulit dengan atau tanpa benjolan
- Nyeri dada
- Kram atau nyeri otot
- Tes darah menunjukkan tingkat potasium yang lebih tinggi dari normal.
Jarang (mempengaruhi kurang dari 1 pasien dalam setiap 100 pasien yang menjalani terapi)
- Masalah keseimbangan (pusing)
- Gatal dan sensasi kulit yang tidak biasa seperti mati rasa, kesemutan, terbakar, menyengat atau menggosok (parestesia)
- Kehilangan atau perubahan selera
- Masalah tidur
- Suasana hati yang tertekan, kecemasan, lebih gugup dari biasanya atau lekas marah
- Hidung tersumbat, kesulitan bernapas atau asma yang memburuk
- Pembengkakan "usus yang disebut" angioedema usus "dan muncul dengan gejala seperti sakit perut, muntah dan diare
- Mulas, sembelit atau mulut kering
- Peningkatan jumlah urin di siang hari
- Lebih banyak berkeringat dari biasanya
- Kehilangan atau penurunan nafsu makan (anoreksia)
- Detak jantung cepat atau tidak teratur.
- Lengan dan kaki bengkak. Ini mungkin pertanda bahwa tubuh Anda menahan lebih banyak air dari biasanya
- Siram
- Penglihatan kabur
- Nyeri pada persendian
- Demam
- Impotensi pada pria, berkurangnya hasrat seksual pada pria dan wanita
- Peningkatan jumlah sel darah putih (eosinofilia) yang ditemukan dalam tes darah
- Perubahan fungsi hati, pankreas atau ginjal ditunjukkan dalam tes darah.
Jarang (mempengaruhi kurang dari 1 pasien dalam setiap 1000 pasien yang menjalani terapi)
- Merasa pingsan atau bingung
- Lidah bengkak dan merah
- Pengelupasan atau pengelupasan kulit yang parah, gatal, ruam pustular
- Masalah kuku (seperti melonggarkan atau memisahkan kuku dari tempatnya)
- Ruam kulit atau memar
- Bintik-bintik pada kulit dan ekstremitas dingin
- Mata merah, bengkak atau berair atau gatal
- Pendengaran terganggu dan telinga berdenging
- Perasaan lemah
- Penurunan jumlah sel darah merah, sel darah putih dan trombosit dalam darah atau konsentrasi hemoglobin, ditunjukkan dalam tes darah.
Sangat jarang (mempengaruhi kurang dari 1 pasien dalam setiap 10.000 pasien yang menjalani terapi)
- Meningkatkan kesadaran tentang matahari.
Efek samping lain yang ditemukan:
Beri tahu dokter Anda jika salah satu kondisi yang dijelaskan di bawah ini menjadi parah atau bertahan lebih dari beberapa hari.
- Sulit berkonsentrasi
- Pembengkakan di mulut
- Tes darah menunjukkan terlalu sedikit sel darah.
- Tes darah menunjukkan natrium darah rendah
- Jari tangan dan kaki yang berubah warna saat kedinginan dan tergelitik atau sakit saat dipanaskan (fenomena Raynaud)
- Pembesaran payudara pada pria
- Reaksi yang diperlambat atau diubah
- Sensasi terbakar
- Perubahan persepsi bau
- Rambut rontok
Jika Anda melihat ada efek samping yang tidak tercantum dalam selebaran ini, beri tahu dokter atau apoteker Anda.
Kadaluwarsa dan Retensi
Jauhkan obat ini dari jangkauan dan pandangan anak-anak. Jangan gunakan Triatec setelah tanggal kedaluwarsa yang tertera pada karton, lepuh dan botol. Tanggal kedaluwarsa mengacu pada hari terakhir bulan yang ditunjukkan.
Obat ini tidak memerlukan kondisi penyimpanan khusus.
Obat-obatan tidak boleh dibuang melalui air limbah atau limbah rumah tangga.
Tanyakan apoteker Anda bagaimana membuang obat-obatan yang tidak lagi Anda gunakan.
Ini akan membantu melindungi lingkungan.
Komposisi dan bentuk farmasi
Apa yang terkandung dalam TRIATEC?
Bahan aktifnya adalah ramipril
1,25 mg: Setiap tablet mengandung 1,25 mg ramipril.
2.5 mg : Tiap tablet mengandung 2.5 mg ramipril
5 mg: Setiap tablet mengandung 5 mg ramipril
10 mg: Tiap tablet mengandung 10 mg ramipril
Bahan lain dari tablet adalah:
1,25 mg dan 10 mg tablet hypromellose, pati jagung pragelatinisasi, selulosa mikrokristalin, natrium stearil fumarat.
2.5 mg tablet hypromellose, pati jagung pregelatinized, selulosa mikrokristalin, natrium stearil fumarat, oksida besi kuning E172.
5 mg tablet hypromellose, pati jagung pragelatinisasi, selulosa mikrokristalin, natrium stearil fumarat, oksida besi merah E172.
Deskripsi seperti apa TRIATEC dan isi paketnya
Tablet 1,25 mg Tablet lonjong, putih sampai putih pudar dengan garis putus-putus, ditandai di atas dengan 1,25 dan logo perusahaan dan di bagian bawah dengan HMN dan 1,25. Garis skor hanya untuk memfasilitasi pemecahan dengan mendukung menelan dan tidak membagi tablet menjadi dosis yang sama.
Tablet 2,5 mg Tablet lonjong, kuning sampai kekuningan dengan garis putus-putus, di sisi atas ditandai dengan 2,5 dan logo perusahaan dan di sisi bawah dengan HMR dan 2,5. Tablet dapat dibagi menjadi bagian yang sama.
Tablet 5 mg Oblong, tablet merah muda dengan garis skor, sisi atas ditandai dengan 5 dan logo perusahaan dan sisi bawah dengan HMP dan 5. Tablet dapat dibagi rata.
Tablet 10 mg Tablet lonjong putih sampai putih pudar dengan garis skor, ditandai di atas dengan HMO / HMO. Tablet dapat dibagi menjadi bagian yang sama.
Tablet Triatec 1,25 mg tersedia dalam kemasan 14, 15, 20, 28, 30, 50, 90, 98, 100 tablet dalam blister PVC / aluminium dan dalam kemasan 500 tablet dalam botol kaca gelap dengan tutup.
Triatec tablet 2,5 mg tersedia dalam kemasan 7, 10, 14, 15, 18, 20, 28, 30, 45, 50, 60, 90, 98, 99, 100, 300, 320, 500 tablet dalam blister PVC / aluminium dan dalam kemasan 500 tablet dalam botol kaca gelap dengan tutup.
Tablet Triatec 5 mg tersedia dalam kemasan 10, 14, 15, 18, 20, 21, 28, 30, 45, 50, 56, 90, 98, 99, 100, 300, 320, 500 tablet dalam blister PVC / aluminium dan dalam kemasan 500 tablet dalam botol kaca gelap dengan penutup.
Tablet Triatec 10 mg tersedia dalam kemasan 7, 10, 14, 15, 18, 20, 28, 30, 45, 50, 56, 90, 98, 99, 100, 300, 320, 500 tablet dalam blister PVC / aluminium dan dalam kemasan 28, 56, 500 tablet dalam botol kaca gelap dengan tutup. Tidak semua ukuran kemasan dapat dipasarkan
Sumber Paket Leaflet: AIFA (Badan Obat Italia). Konten yang diterbitkan pada Januari 2016. Informasi yang ada mungkin tidak up-to-date.
Untuk memiliki akses ke versi terbaru, disarankan untuk mengakses situs web AIFA (Badan Obat Italia). Penafian dan informasi yang berguna.
01.0 NAMA PRODUK OBAT
TABLET TRIATEC
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF
Tablet
Tiap tablet mengandung ramipril 1,25 mg.
Tiap tablet mengandung ramipril 2,5 mg.
Tiap tablet mengandung ramipril 5 mg.
Tiap tablet mengandung ramipril 10 mg.
Untuk daftar lengkap eksipien, lihat bagian 6.1.
03.0 FORMULIR FARMASI
1,25 mg tablet
Tablet lonjong putih sampai putih pudar dengan garis skor, sisi atas ditandai dengan 1,25 dan logo perusahaan dan sisi bawah dengan HMN dan 1,25. Garis skor hanya untuk memfasilitasi pemecahan dengan mendukung menelan dan tidak membagi tablet menjadi dosis yang sama.
tablet 2,5 mg
Tablet lonjong kuning sampai kekuningan dengan garis skor, sisi atas dengan 2,5 dan logo perusahaan dan sisi bawah dengan HMR dan 2,5. Tablet dapat dibagi menjadi bagian yang sama.
5 mg tablet
Tablet berbentuk persegi panjang berwarna merah terang dengan garis skor, sisi atas dengan 5 dan logo perusahaan dan sisi bawah dengan HMP dan 5. Tablet dapat dibagi rata.
10 mg tablet
Tablet lonjong putih sampai putih pudar dengan garis skor, ditandai di sisi atas dengan HMO / HMO. Tablet dapat dibagi menjadi bagian yang sama.
04.0 INFORMASI KLINIS
04.1 Indikasi Terapi
- Pengobatan hipertensi.
- Pencegahan kardiovaskular: pengurangan morbiditas dan mortalitas kardiovaskular pada pasien dengan:
• penyakit kardiovaskular aterotrombotik (penyakit jantung koroner atau stroke sebelumnya, atau penyakit pembuluh darah perifer) atau
• diabetes dengan setidaknya satu faktor risiko kardiovaskular (lihat bagian 5.1)
- Pengobatan penyakit ginjal :
• Nefropati glomerulus diabetik yang baru jadi, ditandai dengan adanya mikroalbuminuria
• Nefropati glomerulus diabetik yang nyata, ditandai dengan makroproteinuria pada pasien dengan setidaknya satu faktor risiko kardiovaskular (lihat bagian 5.1)
• Nefropati non-diabetik glomerulus yang jelas ditandai dengan makroproteinuria 3g / hari (lihat bagian 5.1).
- Pengobatan gagal jantung simtomatik.
- Pencegahan sekunder setelah infark miokard akut: pengurangan kematian setelah fase akut infark miokard pada pasien dengan tanda-tanda klinis gagal jantung ketika dimulai 48 jam setelah onset infark miokard akut
04.2 Posologi dan cara pemberian
Penggunaan lisan.
Dianjurkan agar TRITACE diminum pada waktu yang sama setiap hari.
TRITACE dapat dikonsumsi sebelum, selama atau setelah makan, karena asupan makanan tidak mengubah bioavailabilitasnya (lihat bagian 5.2).
TRIATEC harus ditelan dengan cairan dan tidak boleh dikunyah atau dihancurkan.
Dewasa
Pasien yang diobati dengan diuretik
Hipotensi dapat terjadi setelah memulai pengobatan dengan TRITACE dan lebih mungkin terjadi pada pasien yang diobati secara bersamaan dengan diuretik.Oleh karena itu, hati-hati dianjurkan untuk pasien ini karena mereka dapat mengalami penurunan volume plasma dan / atau garam.
Diuretik harus dihentikan, jika mungkin, 2 atau 3 hari sebelum memulai terapi dengan TRITACE (lihat bagian 4.4).
Pada pasien hipertensi yang diuretiknya belum dihentikan, terapi dengan TRITACE harus dimulai dengan dosis 1,25 mg. Fungsi ginjal dan kalium serum harus dipantau. Dosis TRITACE selanjutnya harus disesuaikan dengan nilai tekanan darah yang diinginkan.
Hipertensi
Dosis harus disesuaikan dengan profil pasien (lihat bagian 4.4) dan kontrol tekanan darah.
TRITACE dapat digunakan sendiri atau dalam kombinasi dengan obat antihipertensi kelas lain (lihat bagian 4.3, 4.4, 4.5 dan 5.1).
Dosis awal
Pengobatan dengan TRITACE harus dimulai secara bertahap, dengan dosis awal yang direkomendasikan 2,5 mg per hari.
Pasien dengan sistem renin-angiotensin-aldosteron yang terlalu aktif mungkin mengalami penurunan tekanan darah yang berlebihan setelah mengambil dosis awal.Untuk pasien ini, dosis awal 1,25 mg dianjurkan, dan memulai pengobatan di bawah pengawasan medis (lihat bagian 4.4) .
Titrasi dan dosis pemeliharaan
Dosis dapat digandakan dengan interval 2-4 minggu untuk secara progresif mencapai nilai tekanan darah yang dibutuhkan; dosis maksimum TRITACE adalah 10 mg per hari. Dosis biasanya diminum sekali sehari.
Pencegahan kardiovaskular
Dosis awal
Dosis awal yang direkomendasikan adalah 2,5 mg TRITACE sekali sehari.
Titrasi dan dosis pemeliharaan
Dosis harus ditingkatkan secara bertahap pada pasien berdasarkan tolerabilitas bahan aktif. Dianjurkan untuk menggandakan dosis setelah satu atau dua minggu pengobatan dan - setelah dua sampai tiga minggu lagi - untuk meningkatkannya sampai target dosis pemeliharaan 10 mg TRITACE sekali sehari tercapai.
Lihat juga posologi yang dijelaskan di atas untuk pasien yang diobati dengan diuretik.
Pengobatan penyakit ginjal
Pada pasien dengan diabetes dan mikroalbuminuria:
Dosis awal
Dosis awal yang dianjurkan adalah 1,25 mg TRITACE sekali sehari.
Titrasi dan dosis pemeliharaan
Dosis harus ditingkatkan secara bertahap pada pasien berdasarkan tolerabilitas bahan aktif.
Direkomendasikan bahwa dosis harian tunggal digandakan menjadi 2,5 mg setelah dua minggu dan dua minggu berikutnya menjadi 5 mg.
Pada pasien dengan diabetes dan setidaknya satu faktor risiko kardiovaskular
Dosis awal
Dosis awal yang direkomendasikan adalah 2,5 mg TRITACE sekali sehari.
Titrasi dan dosis pemeliharaan
Dosis harus ditingkatkan secara bertahap pada pasien berdasarkan tolerabilitas bahan aktif.
Direkomendasikan bahwa dosis harian tunggal digandakan menjadi TRITACE 5 mg setelah satu sampai dua minggu dan kemudian menjadi TRITACE 10 mg setelah dua sampai tiga minggu berikutnya. Target dosis harian adalah 10 mg.
Pada pasien dengan nefropati non-diabetes, didefinisikan oleh makroproteinuria 3g / hari
Dosis awal
Dosis awal yang dianjurkan adalah 1,25 mg TRITACE sekali sehari.
Titrasi dan dosis pemeliharaan
Dosis harus ditingkatkan secara bertahap pada pasien berdasarkan tolerabilitas bahan aktif.
Dianjurkan agar dosis harian tunggal digandakan menjadi 2,5 mg setelah dua minggu dan kemudian menjadi 5 mg setelah dua minggu berikutnya.
Gagal jantung simtomatik
Dosis awal
Pada pasien yang stabil dengan terapi diuretik, dosis awal yang dianjurkan adalah 1,25 mg per hari.
Titrasi dan dosis pemeliharaan
TRITACE harus dititrasi dengan menggandakan dosis setiap satu hingga dua minggu hingga dosis harian maksimum 10 mg. Dua administrasi per hari lebih disukai.
Pencegahan sekunder pada pasien dengan infark miokard akut dan gagal jantung sebelumnya
Dosis awal
Setelah 48 jam infark miokard, pada pasien yang stabil secara klinis dan hemodinamik, dosis awal adalah 2,5 mg dua kali sehari selama tiga hari. Jika dosis awal 2,5 mg tidak dapat ditoleransi, dosis harus diberikan. 1,25 mg dua kali sehari selama dua hari sebelum meningkat menjadi 2,5 mg dan 5 mg dua kali sehari Jika dosis tidak dapat ditingkatkan menjadi 2,5 mg dua kali sehari pengobatan harus dihentikan.
Lihat juga posologi yang dijelaskan di atas untuk pasien yang diobati dengan diuretik.
Titrasi dan dosis pemeliharaan
Dosis harian kemudian ditingkatkan dengan menggandakannya dengan interval satu sampai tiga hari menjadi dosis pemeliharaan 5 mg dua kali sehari.
Bila memungkinkan, dosis pemeliharaan dibagi menjadi dua administrasi per hari.
Jika dosis tidak dapat ditingkatkan menjadi 2.5mg dua kali sehari, pengobatan harus dihentikan. Masih belum cukup pengalaman dalam merawat pasien dengan gagal jantung berat (NYHA IV) segera setelah infark miokard. Jika keputusan dibuat untuk mengobati pasien ini, dianjurkan bahwa terapi dimulai pada 1,25 mg sekali sehari dan perhatian khusus harus dilakukan dalam setiap peningkatan dosis.
populasi khusus
Pasien dengan gangguan fungsi ginjal
Dosis harian pada pasien dengan insufisiensi ginjal harus didasarkan pada bersihan kreatinin (lihat bagian 5.2):
• jika klirens kreatinin 60 ml / menit, tidak perlu menyesuaikan dosis awal (2,5 mg / hari); dosis harian maksimum adalah 10 mg;
• jika klirens kreatinin antara 30-60 ml / menit tidak perlu menyesuaikan dosis awal (2,5 mg / hari); dosis harian maksimum adalah 5 mg;
• jika klirens kreatinin antara 10-30 ml / menit, dosis awal adalah 1,25 mg / hari dan dosis harian maksimum adalah 5 mg;
• Ramipril sulit didialisis pada pasien hipertensi yang menjalani hemodialisis; dosis awal adalah 1,25 mg / hari dan dosis harian maksimum adalah 5 mg; produk obat harus diberikan beberapa jam setelah melakukan dialisis.
Pasien dengan gangguan fungsi hati (lihat bagian 5.2)
Pada pasien dengan insufisiensi hati, pengobatan dengan TRITACE hanya boleh dimulai di bawah pengawasan medis yang ketat dan dosis harian maksimum TRITACE adalah 2,5 mg.
pasien lanjut usia
Dosis awal harus yang terendah dan titrasi berikutnya harus sangat bertahap karena kemungkinan peningkatan efek yang tidak diinginkan terutama pada pasien yang sangat tua atau lemah. Dosis awal ramipril yang dikurangi sebesar 1,25 mg harus dipertimbangkan.
Populasi pediatrik
Keamanan dan kemanjuran ramipril pada anak-anak belum ditetapkan. Data yang tersedia saat ini untuk Triatec dijelaskan di bagian 4.8, 5.1, 5.2 dan 5.3 tetapi tidak ada rekomendasi khusus tentang posology yang dapat dibuat.
04.3 Kontraindikasi
• Hipersensitif terhadap zat aktif, terhadap salah satu eksipien atau terhadap penghambat ACE lainnya (penghambat Enzim Pengubah Angiotensin) (lihat bagian 6.1).
• Riwayat angioedema (herediter, idiopatik, atau angioedema sebelumnya dengan ACE inhibitor atau AIIRA).
• Perawatan ekstrakorporeal yang membuat darah bersentuhan dengan permukaan bermuatan negatif (lihat bagian 4.5).
• Stenosis arteri ginjal bilateral yang signifikan atau stenosis unilateral pada pasien dengan satu ginjal yang berfungsi.
• Kehamilan trimester kedua dan ketiga (lihat bagian 4.4 dan 4.6).
• Ramipril tidak boleh digunakan pada pasien dengan hipotensi atau hemodinamik tidak stabil
• Penggunaan Triatec bersamaan dengan produk yang mengandung aliskiren dikontraindikasikan pada pasien dengan diabetes mellitus atau gangguan ginjal (GFR 2) (lihat bagian 4.5 dan 5.1).
04.4 Peringatan khusus dan tindakan pencegahan yang tepat untuk digunakan
populasi khusus
• Kehamilan
Terapi dengan inhibitor ACE, seperti ramipril atau antagonis reseptor angiotensin II (AIIRA) tidak boleh dimulai selama kehamilan.
Untuk pasien yang merencanakan kehamilan, pengobatan antihipertensi alternatif dengan profil keamanan yang terbukti untuk digunakan pada kehamilan harus digunakan, kecuali terapi lanjutan dengan ACE inhibitor / AIIRA dianggap penting. kehamilan, pengobatan dengan ACE inhibitor / AIIRA harus segera dihentikan, dan, jika sesuai, terapi alternatif harus dimulai (lihat bagian 4.3 dan 4.6).
• Pasien terutama yang berisiko hipotensi
- Pasien dengan aktivasi berlebihan dari sistem renin-angiotensin-aldosteron
Pasien dengan aktivasi berlebihan dari sistem renin-angiotensin-aldosteron berisiko mengalami penurunan tekanan darah akut dan penurunan fungsi ginjal karena penghambatan ACE, terutama ketika inhibitor ACE atau diuretik bersamaan pertama kali diberikan. peningkatan dosis. Aktivasi yang relevan dari sistem renin-angiotensin-aldosteron harus diharapkan dan pengawasan medis termasuk pemantauan tekanan darah diperlukan, misalnya dalam:
• pasien dengan hipertensi berat;
• pasien dengan gagal jantung kongestif dekompensasi;
• pasien dengan hambatan yang signifikan secara hemodinamik terhadap aliran masuk atau keluar ventrikel kiri (misalnya stenosis katup aorta atau mitral);
• pasien dengan stenosis arteri renalis unilateral dengan ginjal kedua yang berfungsi;
• pasien yang mengalami atau mungkin mengalami penipisan cairan atau garam (termasuk pasien yang menggunakan diuretik);
• pasien dengan sirosis hati dan/atau asites;
• selama operasi besar atau selama anestesi dengan obat-obatan yang menyebabkan hipotensi.
Secara umum dianjurkan untuk memperbaiki dehidrasi, hipovolemia atau penipisan garam sebelum memulai pengobatan (namun pada pasien dengan gagal jantung tindakan korektif ini harus dipertimbangkan secara hati-hati terhadap risiko kelebihan beban).
Blokade ganda sistem renin-angiotensin-aldosteron (RAAS)
Terdapat bukti bahwa penggunaan ACE inhibitor, penghambat reseptor angiotensin II atau aliskiren secara bersamaan meningkatkan risiko hipotensi, hiperkalemia, dan penurunan fungsi ginjal (termasuk gagal ginjal akut). Blokade ganda RAAS melalui kombinasi penggunaan ACE inhibitor, penghambat reseptor angiotensin II atau aliskiren tidak direkomendasikan (lihat bagian 4.5 dan 5.1).
Jika terapi blok ganda dianggap mutlak diperlukan, ini hanya boleh dilakukan di bawah pengawasan spesialis dan dengan pemantauan yang ketat dan sering terhadap fungsi ginjal, elektrolit, dan tekanan darah.
ACE inhibitor dan antagonis reseptor angiotensin II tidak boleh digunakan secara bersamaan pada pasien dengan nefropati diabetik.
Gagal jantung sementara atau persisten setelah infark miokard
- Pasien dengan risiko iskemia jantung atau serebral jika terjadi hipotensi akut
Tahap awal pengobatan membutuhkan pengawasan medis yang cermat.
• pasien lanjut usia
Lihat bagian 4.2.
• Operasi
Jika memungkinkan, dianjurkan bahwa pengobatan dengan penghambat enzim pengubah angiotensin seperti ramipril dihentikan satu hari sebelum operasi.
• Pemantauan fungsi ginjal
Fungsi ginjal harus dievaluasi sebelum dan selama pengobatan dan dosis harus disesuaikan terutama pada minggu-minggu pertama pengobatan. Pemantauan yang sangat hati-hati diperlukan pada pasien dengan gangguan ginjal (lihat bagian 4.2). C” adalah risiko gangguan fungsi ginjal, terutama pada pasien gagal jantung kongestif atau setelah transplantasi ginjal.
• Angioedema
Kasus angioedema telah dilaporkan pada pasien yang menerima ACE inhibitor termasuk ramipril (lihat bagian 4.8).
Dalam kasus angioedema, TRITACE harus dihentikan.
Perawatan darurat harus segera dilakukan. Pasien harus diobservasi setidaknya selama 12-24 jam dan dipulangkan hanya setelah gejala sembuh total.
Angioedema usus telah dilaporkan pada pasien yang menerima ACE inhibitor, termasuk TRITACE (lihat bagian 4.8). Pasien-pasien ini datang dengan nyeri perut (dengan atau tanpa mual atau muntah).
• Reaksi anafilaksis selama terapi desensitisasi
Kemungkinan dan keparahan reaksi anafilaksis atau anafilaktoid setelah kontak dengan racun serangga atau alergen lainnya meningkat selama terapi ACE inhibitor. Penghentian sementara TRITACE harus dipertimbangkan sebelum desensitisasi.
• Pemantauan elektrolit: Hiperkalemia
Hiperkalemia telah diamati pada beberapa pasien yang diobati dengan ACE inhibitor termasuk TRITACE. Pasien yang berisiko hiperkalemia antara lain pasien dengan insufisiensi ginjal, usia > 70 tahun, dengan diabetes mellitus yang tidak terkontrol atau mereka yang menggunakan garam kalium, diuretik hemat kalium, atau zat aktif lain yang meningkatkan kadar kalium plasma, atau kondisi seperti dehidrasi, gagal jantung akut. , asidosis metabolik.
Jika penggunaan salah satu zat di atas dianggap perlu, pemantauan rutin kalium serum dianjurkan (lihat bagian 4.5).
• Pemantauan elektrolit: Hiponatremia
Sindrom sekresi hormon anti-diuretik yang tidak tepat (SIADH) dan hiponatremia berikutnya telah diamati pada beberapa pasien yang diobati dengan ramipril. Direkomendasikan bahwa kadar natrium serum dipantau secara teratur pada pasien usia lanjut dan pada pasien lain yang berisiko hiponatremia.
• Neutropenia / agranulositosis
Neutropenia / agranulositosis, serta trombositopenia dan anemia, telah diamati jarang, dan depresi sumsum tulang juga telah dilaporkan.
Disarankan untuk memantau jumlah sel darah putih untuk memungkinkan deteksi kemungkinan leukopenia.
Pemantauan yang lebih sering disarankan pada fase awal pengobatan dan pada pasien dengan gangguan fungsi ginjal, pada pasien dengan kelainan kolagen yang menyertai (misalnya lupus eritematosus atau skleroderma) dan pada mereka yang diobati dengan obat-obatan yang dapat menyebabkan perubahan gambaran darah (lihat paragraf 4.5 dan 4.8).
• Perbedaan etnis
ACE inhibitor menyebabkan insiden angioedema yang lebih tinggi pada pasien kulit hitam dibandingkan pasien non-kulit hitam.
Seperti inhibitor ACE lainnya, ramipril mungkin kurang efektif dalam menurunkan tekanan darah pada populasi kulit hitam dibandingkan populasi non-kulit hitam, mungkin karena prevalensi yang lebih tinggi dari hipertensi renin rendah pada populasi kulit hitam.
• Batuk
Batuk telah dilaporkan dengan penggunaan ACE inhibitor Biasanya, batuk tidak produktif, persisten dan sembuh setelah penghentian terapi. Batuk ACE inhibitor harus dipertimbangkan dalam diagnosis banding batuk.
04.5 Interaksi dengan produk obat lain dan bentuk interaksi lainnya
Data uji klinis menunjukkan bahwa blokade ganda sistem renin-angiotensin-aldosteron (RAAS) melalui penggunaan kombinasi ACE inhibitor, penghambat reseptor angiotensin II atau aliskiren dikaitkan dengan frekuensi efek samping yang lebih tinggi, seperti hipotensi, hiperkalemia, dan penurunan fungsi ginjal (termasuk gagal ginjal akut) dibandingkan dengan penggunaan agen tunggal yang aktif pada sistem RAAS (lihat bagian 4.3, 4.4 dan 5.1).
Asosiasi yang dikontraindikasikan
Perawatan ekstrakorporeal yang menyebabkan kontak antara darah dan permukaan bermuatan negatif seperti dialisis atau hemofiltrasi dengan membran fluks tinggi (misalnya membran poliakrilonitril) atau apheresis lipoprotein densitas rendah dengan menggunakan dekstran sulfat dikontraindikasikan karena peningkatan risiko reaksi anafilaktoid berat (lihat bagian 4.3) Jika jenis pengobatan ini diperlukan, penggunaan membran dialisis yang berbeda atau kelas agen antihipertensi yang berbeda harus dipertimbangkan.
Tindakan pencegahan untuk digunakan
Garam kalium, heparin, diuretik hemat kalium dan zat aktif lainnya yang meningkatkan kadar kalium darah (termasuk antagonis angiotensin II, trimetoprim, takrolimus, siklosporin):
Hiperkalemia dapat terjadi, oleh karena itu pemantauan kadar kalium serum secara hati-hati diperlukan.
Obat antihipertensi (misalnya diuretik) dan obat lain dengan potensi efek antihipertensi (misalnya nitrat, antidepresan trisiklik, anestesi, asupan alkohol, baclofen, alfuzosin, doxazosin, prazosin, tamsulosin, terazosin): Kemungkinan potensiasi risiko hipotensi harus diantisipasi (lihat bagian 4.2 untuk diuretik).
Vasopresor simpatomimetik dan zat lain (misalnya isoproterenol, dobutamide, dopamid, adrenalin) yang dapat mengurangi efek antihipertensi TRIATEC: Pemantauan tekanan darah dianjurkan.
Allopurinol, imunosupresan, kortikosteroid, procainamide, sitostatika dan obat lain yang dapat mengubah gambaran darah: peningkatan risiko reaksi hematologis (lihat bagian 4.4).
garam litium: Ekskresi litium dapat dikurangi dengan ACE inhibitor dan oleh karena itu toksisitas litium dapat ditingkatkan. Kadar litium serum harus dipantau.
Agen antidiabetik termasuk insulin: Reaksi hipoglikemik dapat terjadi. Oleh karena itu, pemantauan glukosa darah dianjurkan.
Obat antiinflamasi nonsteroid dan asam asetilsalisilat: kemungkinan penurunan efek antihipertensi TRITACE harus diantisipasi.Selain itu, terapi bersamaan dengan ACE inhibitor dan NSAID dapat menyebabkan peningkatan risiko perburukan fungsi ginjal dan peningkatan kalaemia.
04.6 Kehamilan dan menyusui
Kehamilan
TRITACE tidak dianjurkan selama trimester pertama kehamilan (lihat bagian 4.4 dan dikontraindikasikan selama trimester kedua dan ketiga kehamilan (lihat bagian 4.3).
Bukti epidemiologis tentang risiko teratogenisitas setelah paparan inhibitor ACE selama trimester pertama kehamilan belum meyakinkan; namun peningkatan kecil dalam risiko tidak dapat dikecualikan.
Untuk pasien yang merencanakan kehamilan, pengobatan antihipertensi alternatif dengan profil keamanan yang terbukti untuk digunakan pada kehamilan harus digunakan kecuali terapi ACE inhibitor lanjutan dianggap penting.
Ketika kehamilan didiagnosis, pengobatan dengan ACE inhibitor harus segera dihentikan dan, jika sesuai, terapi alternatif harus dimulai.
Paparan ACE inhibitor / antagonis reseptor angiortensin II (AIIRA) selama trimester kedua dan ketiga pada wanita diketahui menyebabkan toksisitas janin (penurunan fungsi ginjal, oligohidramnion, retardasi osifikasi tengkorak) dan toksisitas neonatal (gagal ginjal, hipotensi, hiperkalemia) (lihat bagian 5.3 "Data keselamatan praklinis").
Jika paparan ACE inhibitor telah terjadi sejak trimester kedua kehamilan, pemeriksaan ultrasonografi fungsi ginjal dan tengkorak dianjurkan.
Neonatus yang ibunya menggunakan ACE inhibitor harus dipantau secara ketat terhadap hipotensi, oliguria, dan hiperkalemia (lihat juga bagian 4.3 dan 4.4).
Waktunya memberi makan
Karena tidak ada informasi yang cukup tentang penggunaan ramipril selama menyusui (lihat bagian 5.2), TRITACE tidak direkomendasikan dan pengobatan alternatif dengan profil keamanan yang lebih baik selama menyusui lebih disukai, terutama saat menyusui bayi baru lahir atau bayi prematur.
04.7 Efek pada kemampuan mengemudi dan menggunakan mesin
Beberapa efek yang tidak diinginkan (misalnya gejala tekanan darah rendah seperti pusing) dapat mengganggu kemampuan pasien untuk berkonsentrasi dan bereaksi dan oleh karena itu mewakili risiko dalam situasi di mana keterampilan ini sangat penting (misalnya mengoperasikan mesin atau mengemudi kendaraan).
Ini terutama dapat terjadi pada awal pengobatan atau ketika mengganti terapi lain. Setelah dosis pertama atau peningkatan dosis tidak dianjurkan untuk mengemudi atau mengoperasikan mesin selama beberapa jam.
04.8 Efek yang tidak diinginkan
Profil keamanan ramipril termasuk batuk kering persisten dan reaksi akibat hipotensi.Reaksi merugikan yang serius termasuk angioedema, hiperkalemia, gangguan hati atau ginjal, pankreatitis, reaksi kulit yang parah dan neutropenia / agranulositosis.
Frekuensi efek yang tidak diinginkan didefinisikan menggunakan konvensi berikut:
Sangat umum (≥ 1/10); umum (≥ 1/100,
Dalam kelompok frekuensi, efek yang tidak diinginkan terdaftar dalam urutan keparahan.
Populasi pediatrik
Keamanan ramipril dipantau pada 325 anak-anak dan remaja, berusia 2-16 tahun dalam 2 studi klinis. Meskipun sifat dan tingkat keparahan efek samping serupa dengan orang dewasa, frekuensi kejadian berikut lebih tinggi pada anak-anak:
Takikardia, hidung tersumbat dan rinitis, "umum" (yaitu 1/100,
Konjungtivitis "umum" (yaitu 1/100,
Tremor dan urtikaria "jarang" (yaitu 1/1000,
Profil keamanan keseluruhan untuk ramipril pada pasien anak tidak berbeda secara signifikan dari profil keamanan pada orang dewasa.
04.9 Overdosis
Gejala yang terkait dengan overdosis ACE inhibitor mungkin termasuk vasodilatasi perifer yang berlebihan (dengan ditandai hipotensi, syok), bradikardia, gangguan elektrolit, gagal ginjal.Pasien harus dipantau secara hati-hati dan pengobatan harus simtomatik dan suportif. Tindakan utama yang disarankan meliputi detoksifikasi (bilas lambung, pemberian adsorben) dan tindakan untuk memulihkan stabilitas hemodinamik, termasuk pemberian agonis adrenal alfa 1 atau angiotensin II (angiotensinamide).Ramiprilat, metabolit aktif ramipril, kurang dihilangkan dari sirkulasi umum dengan hemodialisis.
05.0 SIFAT FARMAKOLOGIS
05.1 Sifat farmakodinamik
Kelompok farmakoterapi: ACE inhibitor; Kode A.T.C: C09AA05
Mekanisme aksi .
Ramiprilat, metabolit aktif dari prodrug ramipril, menghambat enzim dipeptidylcarboxypeptidase I (sinonim: enzim pengubah angiotensin; kininase II). Enzim ini, pada tingkat plasma dan jaringan, menentukan konversi angiotensin I menjadi zat vasokonstriktor angiotensin II , dan degradasi bradikinin vasodilator Penurunan pembentukan angiotensin II dan penghambatan degradasi bradikinin menyebabkan vasodilatasi.
Karena angiotensin II juga merangsang pelepasan aldosteron, ramiprilat menyebabkan penurunan sekresi aldosteron.
Respon rata-rata terhadap ACE inhibitor pada pasien hipertensi kulit hitam (Afro-Karibia) (biasanya populasi hipertensi ini memiliki tingkat renin yang rendah) lebih rendah daripada pasien non-kulit hitam.
Efek farmakodinamik .
Sifat antihipertensi:
Pemberian ramipril menyebabkan penurunan yang nyata pada resistensi arteri perifer. Umumnya baik aliran plasma ginjal maupun filtrasi glomerulus tidak mengalami perubahan yang mencolok.
Pemberian ramipril pada pasien hipertensi menghasilkan penurunan tekanan darah pada posisi berdiri dan terlentang, tanpa kompensasi peningkatan denyut jantung.
Setelah dosis oral tunggal, pada kebanyakan pasien aksi antihipertensi terjadi setelah 1 atau 2 jam dari asupan, mencapai efek maksimum setelah 3-6 jam dan berlangsung setidaknya selama 24 jam.
Efek antihipertensi maksimum dari pengobatan berkelanjutan dengan ramipril umumnya dicapai setelah 3-4 minggu pengobatan.
Telah terbukti bahwa efek antihipertensi dipertahankan untuk terapi jangka panjang hingga 2 tahun.
Penghentian terapi secara tiba-tiba tidak menyebabkan peningkatan tekanan darah yang cepat.
Gagal jantung:
Ramipril telah terbukti efektif, selain terapi konvensional dengan diuretik dan glikosida jantung, pada pasien dengan kelas fungsional II-IV yang ditentukan oleh New-York Heart Association. Obat ini memiliki efek menguntungkan pada hemodinamik jantung (penurunan tekanan pengisian ventrikel kiri dan kanan, penurunan resistensi pembuluh darah perifer total, peningkatan curah jantung, dan peningkatan indeks jantung). Ini juga mengurangi aktivasi neuroendokrin.
Kemanjuran dan keamanan klinis
Pencegahan kardiovaskular / nefroproteksi:
Sebuah studi pencegahan terkontrol plasebo (studi HOPE) dilakukan di mana ramipril ditambahkan ke terapi standar di lebih dari 9.200 pasien. Pasien dengan peningkatan risiko penyakit kardiovaskular akibat penyakit kardiovaskular aterotrombotik (penyakit arteri koroner, stroke atau penyakit pembuluh darah perifer) atau diabetes mellitus dengan setidaknya satu faktor risiko tambahan (mikroalbuminuria, hipertensi, kadar kolesterol total tinggi, kadar kolesterol HDL rendah, atau merokok), dimasukkan dalam penelitian ini.
Studi menunjukkan bahwa ramipril secara statistik secara signifikan menurunkan kejadian infark miokard, kematian kardiovaskular dan stroke, sendiri atau gabungan (gabungan peristiwa utama).
Studi HARAPAN: hasil utama
Studi MICRO - HOPE, substudi yang telah ditentukan dari studi HOPE, mengevaluasi efek penambahan ramipril 10 mg pada rejimen saat ini versus plasebo pada 3.577 pasien berusia 55 tahun (tanpa batas usia atas), mayoritas dengan diabetes tipe 2 ( dan setidaknya satu faktor risiko CV lainnya) normotensif atau hipertensi.
Analisis utama dari hasil menunjukkan bahwa 117 (6,5%) peserta yang diobati dengan ramipril dan 149 (8,4%) yang diobati dengan plasebo mengembangkan nefropati terbuka, yang sesuai dengan Relative Risk Reduction (RRR) sebesar 24%.; 95% CI [3 -40], p = 0,027.
Penelitian REIN acak, tersamar ganda, kelompok paralel, terkontrol plasebo bertujuan untuk menunjukkan efek pengobatan ramipril pada tingkat penurunan fungsi glomerulus (GFR) pada 352 pasien normotensif atau hipertensi (18-70 tahun). usia) dengan proteinuria ringan (yaitu ekskresi protein urin> 1 e
Analisis utama pasien dengan proteinuria paling parah (lapisan terpisah sebelum waktunya karena manfaat yang terlihat pada kelompok ramipril) menunjukkan bahwa tingkat rata-rata penurunan GFR per bulan lebih rendah dengan ramipril dibandingkan dengan plasebo; -0, 54 vs. - 0,88 mL / menit / bulan, p = 0,038. Perbedaan antara kelompok adalah 0,34 [0,03-0,65] per bulan, dan sekitar 4 mL / menit / tahun; pada 23, 1% pasien dalam kelompok ramipril mencapai titik akhir sekunder gabungan dari dua kali lipat konsentrasi serum kreatinin awal dan / atau gagal ginjal stadium akhir (ESRD) (kebutuhan untuk dialisis atau transplantasi ginjal) dibandingkan 45,5% pada plasebo (p = 0,02).
Blokade ganda sistem renin-angiotensin-aldosteron (RAAS):
Dua uji coba terkontrol secara acak besar (ONTARGET (Ongoing Telmisartan Alone dan dalam kombinasi dengan Ramipril Global Endpoint Trial) dan VA Nephron-D (The Veterans Affairs Nephropathy in Diabetes)) telah meneliti penggunaan kombinasi ACE inhibitor dengan antagonis reseptor angiotensin II.
ONTARGET adalah penelitian yang dilakukan pada pasien dengan riwayat penyakit kardiovaskular atau serebrovaskular, atau diabetes mellitus tipe 2 yang terkait dengan bukti kerusakan organ. VA NEPHRON-D adalah penelitian yang dilakukan pada pasien dengan diabetes mellitus tipe 2 dan nefropati diabetik.
Studi-studi ini tidak menunjukkan efek menguntungkan yang signifikan pada hasil dan kematian ginjal dan / atau kardiovaskular, sementara peningkatan risiko hiperkalemia, cedera ginjal akut dan / atau hipotensi diamati dibandingkan dengan monoterapi.
Hasil ini juga relevan untuk ACE inhibitor dan antagonis reseptor angiotensin II lainnya, mengingat sifat farmakodinamiknya yang serupa.
Oleh karena itu, ACE inhibitor dan antagonis reseptor angiotensin II tidak boleh digunakan secara bersamaan pada pasien dengan nefropati diabetik.
ALTITUDE (Aliskiren Trial in Type 2 Diabetes Using Cardiovascular and Renal Disease Endpoints) adalah penelitian yang bertujuan untuk memverifikasi keuntungan penambahan aliskiren pada terapi standar ACE inhibitor atau antagonis reseptor angiotensin II pada pasien dengan diabetes mellitus tipe 2 dan penyakit ginjal kronis. , penyakit kardiovaskular, atau keduanya. Penelitian dihentikan lebih awal karena peningkatan risiko efek samping. Kematian kardiovaskular dan stroke keduanya secara numerik lebih sering pada kelompok aliskiren daripada kelompok plasebo, dan efek samping dan efek samping serius yang menarik ( hiperkalemia, hipotensi dan disfungsi ginjal) dilaporkan lebih sering pada kelompok aliskiren daripada kelompok plasebo.
Pencegahan sekunder setelah infark miokard akut
Studi AIRE melibatkan lebih dari 2.000 pasien dengan tanda klinis sementara/persisten dari gagal jantung setelah didokumentasikan infark miokard. Pengobatan ramipril dimulai 3-10 hari setelah infark miokard akut.Penelitian menunjukkan bahwa setelah waktu tindak lanjut rata-rata 15 bulan, mortalitas pada pasien yang diobati dengan ramipril adalah 16,9% sedangkan pada pasien yang diobati dengan ramipril, yang diobati dengan plasebo adalah 22,6%, yang berarti pengurangan absolut dalam kematian sebesar 5,7% dan pengurangan risiko relatif sebesar 27% (CI 95% [11- 40%]).
Populasi pediatrik
Dalam uji klinis acak, double-blind, terkontrol plasebo yang melibatkan 244 pasien anak dengan hipertensi (73% hipertensi primer), berusia 6-16 tahun, pasien menerima ramipril dosis rendah, sedang atau tinggi berdasarkan berat badan untuk mencapai ramiprilat plasma. konsentrasi yang sesuai dengan dosis dewasa 1,25 mg, 5 mg dan 20 mg. Pada akhir 4 minggu, ramipril tidak efektif dalam menurunkan tekanan darah sistolik, tetapi pada dosis yang lebih tinggi menurunkan tekanan darah diastolik. Ramipril dosis menengah dan tinggi menunjukkan penurunan yang signifikan pada tekanan darah sistolik dan diastolik pada anak-anak dengan hipertensi yang dikonfirmasi.
Efek ini tidak diamati dalam studi klinis acak, double-blind, peningkatan dosis, berhenti setelah 4 minggu pada 218 pasien anak berusia 6-16 tahun (75% hipertensi primer), di mana tekanan sistolik dan diastolik menunjukkan rebound sederhana, tetapi tidak kembali signifikan secara statistik ke baseline, di ketiga tingkat dosis ramipril yang diuji berat [dosis rendah (0,625 mg - 2,5 mg), dosis sedang (2,5 mg) mg - 10 mg) atau dosis tinggi (5 mg - 20 mg)]. Ramipril tidak menunjukkan hubungan dosis/respon linier pada populasi anak yang diteliti.
05.2 Sifat farmakokinetik
Farmakokinetik dan Metabolisme
Penyerapan
Setelah pemberian oral, ramipril diserap dengan cepat dari saluran pencernaan: konsentrasi plasma puncak ramipril tercapai dalam 1 jam Berdasarkan pemulihan urin, penyerapan setidaknya 56% dan tidak terpengaruh secara signifikan oleh adanya makanan di saluran pencernaan. Bioavailabilitas metabolit aktif ramiprilat setelah pemberian oral 2,5 mg dan 5 mg ramipril adalah 45%.
Konsentrasi plasma puncak ramiprilat, satu-satunya metabolit aktif ramipril, dicapai 2-4 jam setelah asupan ramipril.Konsentrasi plasma ramiprilat stabil setelah pemberian sekali sehari dari dosis harian biasa ramipril dicapai pada hari keempat pengobatan kira-kira .
Distribusi
Pengikatan protein serum ramipril sekitar 73% dan ramiprilat sekitar 56%.
Metabolisme
Ramipril hampir sepenuhnya dimetabolisme menjadi ramiprilat dan ester diketopiperazine, bentuk asam dari diketopiperazine dan glukuronida dari ramipril dan ramiprilat.
Eliminasi
Ekskresi metabolit terutama melalui ginjal.
Konsentrasi plasma ramiprilat menurun secara polifasik. Karena ikatannya yang kuat dan jenuh dengan ACE dan disosiasi yang lambat dari enzim, ramiprilat menunjukkan fase eliminasi terminal yang berkepanjangan pada konsentrasi plasma yang sangat rendah.
Setelah beberapa dosis harian ramipril, waktu paruh efektif konsentrasi ramiprilat adalah 13-17 jam untuk dosis 5-10 mg dan lebih lama untuk dosis rendah 1,25-2,5 mg. mengikat ramiprilat.
Dosis oral tunggal ramipril menghasilkan tingkat ramipril yang tidak terdeteksi dan metabolitnya dalam ASI. Namun, efek pemberian dosis ganda tidak diketahui.
Pasien dengan insufisiensi ginjal (lihat bagian 4.2)
Ekskresi ramiprilat ginjal berkurang pada pasien dengan insufisiensi ginjal dan pembersihan ginjal ramiprilat sebanding dengan bersihan kreatinin.Hal ini menyebabkan peningkatan konsentrasi plasma ramiprilat yang menurun lebih lambat dibandingkan pada pasien dengan fungsi ginjal normal.
Pasien dengan insufisiensi hati (lihat bagian 4.2)
Pada pasien dengan gangguan fungsi hati, metabolisme ramipril menjadi ramiprilat tertunda karena penurunan aktivitas esterase hati; pada pasien ini, kadar plasma ramipril meningkat.Konsentrasi puncak ramiprilat pada pasien ini, bagaimanapun, tidak berbeda dari yang terlihat pada subjek dengan fungsi hati normal.
Waktunya memberi makan
Dosis oral tunggal ramipril menghasilkan tingkat ramipril yang tidak terdeteksi dan metabolitnya dalam ASI. Namun, efek pemberian dosis ganda tidak diketahui.
Populasi pediatrik
Profil farmakokinetik ramipril dipelajari pada 30 pasien pediatrik hipertensi, berusia 2 hingga 16 tahun, dengan berat 10 kg. Setelah pemberian dosis 0,05 hingga 0,2 mg / kg, ramipril dengan cepat dan sebagian besar dimetabolisme menjadi ramiprilat. Konsentrasi plasma puncak ramiprilat terjadi dalam 2-3 jam. Pembersihan ramiprilat sangat berkorelasi dengan log berat badan (p
05.3 Data keamanan praklinis
Pemberian oral ramipril ditemukan tanpa toksisitas akut pada hewan pengerat dan anjing. Studi yang melibatkan pemberian oral kronis dilakukan pada tikus, anjing dan monyet. Perubahan elektrolit plasma terdeteksi pada ketiga spesies. Sebagai ekspresi aktivitas farmakodinamik ramipril, pembesaran nyata aparatus juxtaglomerular ditemukan pada anjing dan monyet dimulai dengan dosis harian 250 mg / kg. Tikus, anjing dan monyet ditoleransi dosis harian masing-masing 2, 2,5 dan 8 mg / kg tanpa efek samping.
Kerusakan ginjal yang ireversibel diamati pada tikus yang sangat muda yang diobati dengan ramipril dosis tunggal.
Studi toksikologi reproduksi pada tikus, kelinci dan monyet mengungkapkan tidak ada sifat teratogenik. Kesuburan tidak terpengaruh pada tikus jantan atau betina.
Pemberian ramipril pada tikus betina selama masa kehamilan dan menyusui mengakibatkan kerusakan ginjal ireversibel (pelebaran pelvis ginjal) pada keturunannya pada dosis harian 50 mg / kg berat badan atau lebih tinggi.
Uji mutagenisitas, yang dilakukan dengan menggunakan berbagai sistem uji, tidak memberikan bukti bahwa ramipril memiliki sifat mutagenik atau genotoksik.
06.0 INFORMASI FARMASI
06.1 Eksipien
1,25 mg tablet
hypromellose, pati jagung pragelatinisasi, selulosa mikrokristalin, natrium stearil fumarat.
tablet 2,5 mg
hypromellose, pati jagung pragelatinisasi, selulosa mikrokristalin, natrium stearil fumarat, oksida besi kuning E172.
5 mg tablet
hypromellose, pati jagung pragelatinisasi, selulosa mikrokristalin, natrium stearil fumarat, oksida besi merah E 172.
10 mg tablet
hypromellose, pati jagung pragelatinisasi, selulosa mikrokristalin, natrium stearil fumarat.
06.2 Ketidakcocokan
Tidak berhubungan.
06.3 Masa berlaku
3 tahun.
06.4 Tindakan pencegahan khusus untuk penyimpanan
Obat ini tidak memerlukan kondisi penyimpanan khusus
06.5 Sifat kemasan langsung dan isi kemasan
1,25 mg: bungkus 14, 15, 20, 28, 30, 50, 90, 98, 100 tablet dalam lepuh PVC / aluminium
2.5 mg: bungkus 7, 10, 14, 15, 18, 20, 28, 30, 45, 50, 60, 90, 98, 99, 100, 300, 320, 500 tablet dalam lepuh PVC / aluminium,
5 mg: bungkus 10, 14, 15, 18, 20, 21, 28, 30, 45, 50, 56, 90, 98, 99, 100, 300, 320, 500 tablet dalam lepuh PVC / aluminium
10 mg: bungkus 7, 10, 14, 15, 18, 20, 28, 30, 45, 50, 56, 90, 98, 99, 100, 300, 320, 500 tablet dalam lepuh PVC / aluminium
1,25 mg: 500 tablet dalam botol kaca gelap tipe III (Eur.Ph.) dengan tutup ulir HDPE.
2.5 mg: 500 tablet dalam botol kaca gelap tipe III (Eur.Ph.) dengan tutup ulir HDPE.
5 mg: 500 tablet dalam botol kaca gelap tipe III (Eur.Ph.) dengan tutup ulir HDPE.
10 mg: 25, 56, 500 tablet dalam botol kaca gelap tipe III (Eur.Ph.) dengan tutup ulir HDPE.
Tidak semua ukuran kemasan dapat dipasarkan.
06.6 Petunjuk penggunaan dan penanganan
Obat yang tidak terpakai dan limbah yang berasal dari obat ini harus dibuang sesuai dengan peraturan setempat.
07.0 PEMEGANG OTORITAS PEMASARAN
Sanofi S.p.A. - Viale L. Bodio, 37 / B - 20158 Milan
08.0 NOMOR OTORITAS PEMASARAN
"tablet 1,25 mg" - 28 tablet dalam PVC / AL A.I.C. n.: 027161049
"Tablet 2,5 mg" - 28 tablet yang dapat dibagi dalam PVC / AL A.I.C. n.: 027161052
"2.5 mg tablet" - 320 tablet yang dapat dibagi dalam PVC / AL A.I.C. n.: 027161088
"5 mg tablet" - 14 tablet yang dapat dibagi dalam PVC / AL A.I.C. n.: 027161064
"5 mg tablet" - 320 tablet yang dapat dibagi dalam PVC / AL A.I.C. n.: 027161090 "tablet 10 mg" - 28 tablet yang dapat dibagi dalam PVC / AL A.I.C. n.: 027161076
"10 mg tablet" - 320 tablet yang dapat dibagi dalam PVC / AL A.I.C. n.: 027161102
09.0 TANGGAL OTORISASI PERTAMA ATAU PEMBARUAN KUASA
Tanggal Otorisasi Pertama: 1 Maret 1990 Triatec 1,25 mg, 2,5 mg, 5 mg.
23 Februari 2004 Triatec 10 mg
Tanggal perpanjangan terakhir: 01 Juni 2010
10.0 TANGGAL REVISI TEKS
Mei 2015














.jpg)





.jpg)





