Bahan aktif: Lenalidomide
Revlimid kapsul keras 2,5 mg
Revlimid kapsul keras 5 mg
Revlimid kapsul keras 7,5 mg
Revlimid kapsul keras 10 mg
Revlimid kapsul keras 15 mg
Revlimid kapsul keras 20 mg
Revlimid kapsul keras 25 mg
Mengapa Revlimid digunakan? Untuk apa?
Revlimid mengandung zat aktif "lenalidomide". Obat ini termasuk dalam kelompok obat yang mempengaruhi fungsi sistem kekebalan tubuh.
Revlimid digunakan pada orang dewasa untuk:
- Mieloma multipel
- Sindrom mielodisplastik
- Limfoma sel mantel
Multiple myeloma dan Revlimid
Multiple myeloma adalah jenis kanker yang mempengaruhi jenis sel darah putih tertentu, yang disebut sel plasma. Sel-sel ini berkumpul di sumsum tulang dan membelah tak terkendali. Hal ini dapat merusak tulang dan ginjal.
Multiple myeloma biasanya tidak dapat disembuhkan. Namun, tanda dan gejalanya bisa sangat berkurang atau hilang untuk beberapa waktu. Hasil ini disebut "respon".
Dalam pengobatan multiple myeloma, Revlimid digunakan dalam kombinasi dengan obat lain.
Revlimid pada pasien dengan multiple myeloma yang baru didiagnosis
Revlimid hanya digunakan pada pasien yang baru didiagnosis ketika mereka tidak dapat menjalani transplantasi sumsum tulang.
Jika Anda berusia 75 tahun atau lebih atau memiliki masalah ginjal sedang hingga berat, dokter Anda akan memeriksa Anda dengan cermat sebelum memulai perawatan.
Ada dua jenis perawatan pada pasien yang baru didiagnosis:
- Revlimid bersama dengan obat anti-inflamasi yang disebut 'dexamethasone'.
- Revlimid bersama dengan obat kemoterapi yang disebut 'melphalan' dan obat imunosupresif yang disebut 'prednison'. Anda akan meminum obat-obatan lain ini pada awal pengobatan dan kemudian melanjutkan penggunaan Revlimid saja.
Revlimid pada pasien dengan multiple myeloma yang telah memiliki setidaknya satu jenis pengobatan sebelumnya
- Revlimid diambil bersama dengan obat anti-inflamasi yang disebut 'dexamethasone'.
Revlimid dapat menghentikan tanda dan gejala multiple myeloma agar tidak semakin parah. Ini juga telah terbukti menunda kembalinya multiple myeloma setelah perawatan.
Sindrom Myelodysplastic dan Revlimid
Sindrom myelodysplastic (MDS) adalah kumpulan dari banyak penyakit yang berbeda dari darah dan sumsum tulang. Sel darah menjadi abnormal dan tidak berfungsi dengan baik. Pasien dapat memiliki berbagai tanda dan gejala, termasuk jumlah sel darah merah yang rendah (anemia), kebutuhan akan transfusi darah, dan risiko infeksi.
Revlimid sendiri digunakan untuk mengobati pasien dewasa yang didiagnosis dengan sindrom myelodysplastic yang memiliki semua kondisi berikut:
- jika Anda memerlukan transfusi darah secara teratur untuk mengobati tingkat sel darah merah yang rendah ("anemia yang bergantung pada transfusi")
- jika Anda memiliki "kelainan sel sumsum tulang yang disebut" kelainan sitogenetik penghapusan 5q terisolasi. "Ini berarti tubuh Anda tidak menghasilkan cukup sel darah sehat
- jika perawatan lain yang digunakan sebelumnya tidak cocok atau tidak cukup efektif.
Revlimid dapat meningkatkan jumlah sel darah merah sehat yang diproduksi oleh tubuh dengan mengurangi jumlah sel abnormal:
- Hal ini dapat mengurangi jumlah transfusi darah yang dibutuhkan. Tidak ada transfusi mungkin diperlukan.
Limfoma sel mantel dan Revlimid
Limfoma sel mantel adalah kanker jaringan limfatik (bagian dari sistem kekebalan tubuh), yang mempengaruhi jenis sel darah putih yang disebut limfosit B. Pada limfoma sel mantel, limfosit B tumbuh di luar kendali dan menumpuk di jaringan getah bening, sumsum tulang , atau darah .
Revlimid digunakan sendiri untuk mengobati pasien dewasa yang didiagnosis dengan limfoma sel mantel yang sebelumnya tidak diobati.
Bagaimana Revlimid bekerja?
Revlimid bekerja pada sistem kekebalan tubuh dan langsung pada tumor dalam beberapa cara:
- menghentikan perkembangan sel kanker
- menghentikan pertumbuhan pembuluh darah yang membawa darah ke sel tumor
- dengan merangsang bagian dari sistem kekebalan tubuh untuk menyerang sel kanker.
Kontraindikasi Ketika Revlimid tidak boleh digunakan
Jangan minum Revlimid
- Jika Anda sedang hamil atau berpikir Anda sedang hamil, atau jika Anda berencana untuk hamil, karena Revlimid diperkirakan akan berbahaya bagi bayi yang belum lahir (lihat bagian 2, "Peringatan dan tindakan pencegahan" dan "Kehamilan dan menyusui").
- Jika ada kemungkinan Anda hamil kecuali Anda mengambil semua tindakan yang diperlukan untuk menghindari kehamilan (lihat bagian 2 "Peringatan dan tindakan pencegahan" dan "Kehamilan dan menyusui"). Jika ada kemungkinan Anda hamil, dokter Anda akan mencatat dan mengkonfirmasi dengan setiap resep bahwa tindakan yang diperlukan untuk menghindari kehamilan telah diambil.
- Jika Anda alergi terhadap lenalidomide atau salah satu bahan lain dari obat ini (tercantum di bagian 6). Jika Anda merasa alergi, mintalah saran dari dokter Anda.
Jika salah satu dari ini berlaku untuk Anda, jangan gunakan Revlimid. Jika ragu, konsultasikan dengan dokter Anda.
Kewaspadaan penggunaan Apa yang perlu Anda ketahui sebelum menggunakan Revlimid
Beri tahu dokter Anda sebelum memulai perawatan jika:
- Anda pernah mengalami episode pembekuan darah di masa lalu karena risiko pembekuan darah di pembuluh darah dan arteri meningkat selama perawatan
- memiliki tanda-tanda infeksi, seperti batuk atau demam
- Anda memiliki masalah ginjal - dokter Anda dapat mengubah dosis Revlimid
- pernah mengalami serangan jantung, mengalami pembekuan darah, atau jika Anda merokok, memiliki tekanan darah tinggi atau kadar kolesterol tinggi
- memiliki beban tumor yang tinggi di seluruh tubuh, termasuk di sumsum tulang. Hal ini dapat menyebabkan penyakit di mana tumor rusak dan menyebabkan tingkat bahan kimia yang tidak biasa dalam darah, yang dapat menyebabkan gagal ginjal (penyakit ini terjadi disebut "tumor sindrom lisis")
- memiliki reaksi alergi selama pengobatan dengan thalidomide, seperti ruam, gatal, bengkak, pusing atau kesulitan bernafas
Jika salah satu dari ini berlaku untuk Anda, beri tahu dokter Anda sebelum memulai perawatan.
Jika Anda memiliki sindrom myelodysplastic, Anda lebih mungkin mengembangkan penyakit yang lebih lanjut yang disebut leukemia myeloid akut (AML). Selanjutnya, peran Revlimid pada kemungkinan mengembangkan AML tidak diketahui.Dokter Anda mungkin meminta Anda untuk beberapa tes untuk memeriksa tanda-tanda yang dapat lebih akurat memprediksi kemungkinan mengembangkan AML selama pengobatan dengan Revlimid.
Analisis dan kontrol
Anda akan menjalani tes darah secara teratur sebelum dan selama perawatan dengan Revlimid, karena Revlimid dapat menyebabkan pengurangan sel darah yang melindungi Anda dari infeksi (sel darah putih) dan sel yang membantu pembekuan darah (trombosit). Dokter Anda akan meminta Anda untuk melakukan tes darah:
- sebelum pengobatan
- setiap minggu selama 8 minggu pertama pengobatan (untuk pasien dengan limfoma sel mantel, ini akan terjadi setiap 2 minggu pada siklus 3 dan 4 dan kemudian pada awal setiap siklus)
- setidaknya sebulan sekali setelahnya.
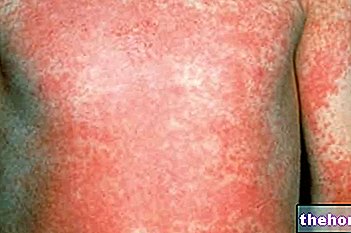
Dokter Anda mungkin memeriksa perubahan pada kulit Anda, seperti bintik-bintik merah atau ruam.
Dokter Anda mungkin memutuskan untuk menyesuaikan dosis Revlimid atau menghentikan pengobatan tergantung pada hasil tes darah dan kondisi umum Anda. Jika Anda adalah pasien yang baru didiagnosis, dokter Anda mungkin juga mengevaluasi pengobatan berdasarkan usia Anda dan kondisi lain yang mungkin sudah ada.
Donor darah
Anda tidak boleh mendonorkan darah selama terapi lenalidomide dan selama satu minggu setelah menghentikan pengobatan.
Anak-anak dan remaja
Revlimid tidak dianjurkan untuk digunakan pada anak-anak dan remaja di bawah usia 18 tahun.
Interaksi Obat atau makanan mana yang dapat mengubah efek Revlimid
Beri tahu dokter atau perawat Anda jika Anda sedang mengonsumsi, baru saja mengonsumsi atau mungkin mengonsumsi obat lain, termasuk yang diperoleh tanpa resep dan obat herbal.Hal ini karena Revlimid dapat memengaruhi cara kerja beberapa obat lain, dan beberapa obat lain dapat memengaruhi cara kerja Revlimid. .
Secara khusus, beri tahu dokter atau perawat Anda jika Anda sedang mengonsumsi obat-obatan berikut:
- beberapa obat yang digunakan untuk mencegah kehamilan, seperti kontrasepsi oral, karena mungkin tidak lagi efektif
- beberapa obat yang digunakan untuk masalah jantung, seperti digoxin
- beberapa obat yang digunakan untuk mengencerkan darah, seperti warfarin
Peringatan Penting untuk diketahui bahwa:
Kehamilan, menyusui dan kontrasepsi - informasi untuk wanita dan pria
Kehamilan
Untuk wanita yang menggunakan Revlimid
- Anda tidak boleh mengonsumsi Revlimid jika Anda sedang hamil, karena obat ini diperkirakan berbahaya bagi bayi yang belum lahir.
- Anda tidak boleh hamil saat dirawat dengan Revlimid. Jika ada kemungkinan hamil, Anda harus menggunakan metode kontrasepsi yang efektif (lihat bagian "Kontrasepsi").
- Jika Anda hamil saat menggunakan Revlimid, Anda harus segera menghentikan pengobatan dan memberi tahu dokter Anda.
Untuk pria yang menggunakan Revlimid
- Jika pasangan Anda hamil saat Anda menggunakan Revlimid, segera beri tahu dokter Anda. Juga disarankan agar pasangan Anda menghubungi dokter Anda.
- Selain itu, Anda harus menggunakan metode kontrasepsi yang efektif (lihat bagian "Kontrasepsi").
Waktunya memberi makan
Anda tidak boleh menyusui saat menggunakan Revlimid, karena tidak diketahui apakah obat ini masuk ke dalam ASI.
Kontrasepsi
Untuk wanita yang menggunakan Revlimid
Sebelum memulai perawatan, Anda harus bertanya kepada dokter Anda apakah ada kemungkinan bagi Anda untuk hamil, bahkan jika menurut Anda itu tidak mungkin.
Jika ada kemungkinan Anda akan hamil
- Anda harus menjalani tes kehamilan di bawah pengawasan dokter Anda (sebelum setiap perawatan, setiap 4 minggu selama perawatan dan 4 minggu setelah akhir perawatan) kecuali dalam kasus di mana telah dipastikan bahwa saluran tuba telah dipotong dan ditutup, untuk mencegah telur dari mencapai rahim (sterilisasi dengan mengikat tabung)
- Anda harus menggunakan metode kontrasepsi yang efektif selama 4 minggu sebelum memulai pengobatan, selama pengobatan dan hingga 4 minggu setelah menghentikan pengobatan.Dokter Anda akan memberi tahu Anda tentang metode kontrasepsi yang sesuai.
Untuk pria yang menggunakan Revlimid
Revlimid masuk ke dalam air mani manusia. Jika ada kemungkinan pasangan Anda hamil atau hamil dan dia tidak menggunakan metode kontrasepsi yang efektif, Anda harus menggunakan kondom selama perawatan dan selama satu minggu setelah akhir perawatan, bahkan jika Anda telah menjalani vasektomi. .
Mengemudi dan menggunakan mesin
Jangan mengemudi atau mengoperasikan mesin jika Anda merasa pusing, lelah, mengantuk, pusing, atau penglihatan kabur.
Revlimid mengandung laktosa
Revlimid mengandung laktosa. Jika Anda telah diberitahu oleh dokter Anda bahwa Anda memiliki "intoleransi terhadap beberapa gula, hubungi dokter Anda sebelum mengambil Revlimid.
Dosis, Cara dan Waktu Pemberian Cara Pemakaian Revlimid: Posology
Revlimid harus diberikan oleh profesional kesehatan yang berpengalaman dalam pengobatan multiple myeloma atau sindrom myelodysplastic dan limfoma sel mantel.
- Ketika digunakan untuk mengobati multiple myeloma, Revlimid digunakan dalam kombinasi dengan obat-obatan lain (lihat bagian 1 'Apa' Revlimid itu dan untuk apa kegunaannya ').
- Ketika digunakan untuk pengobatan sindrom myelodysplastic dan limfoma sel mantel, Revlimid dikonsumsi sendiri.
Selalu minum Revlimid sendiri atau Revlimid dalam kombinasi dengan obat lain, selalu ikuti petunjuk dokter dengan tepat. Jika ragu, konsultasikan dengan dokter atau apoteker Anda.
Jika Anda mengonsumsi Revlimid dalam kombinasi dengan obat-obatan lain, silakan berkonsultasi dengan selebaran paket obat-obatan tersebut untuk informasi lebih lanjut tentang penggunaan dan efeknya.
Siklus pengobatan
- Revlimid dan obat-obatan yang perlu Anda konsumsi dalam kombinasi dengan Revlimid diambil selama beberapa hari selama 4 minggu (28 hari).
- Setiap periode 28 hari disebut "siklus pengobatan".
- Tergantung pada hari menstruasi Anda, Anda akan minum satu atau lebih obat. Namun, dalam beberapa hari Anda tidak akan minum obat apa pun.
- Setelah setiap siklus 28 hari selesai, "siklus" baru harus dimulai selama 28 hari ke depan.
Dosis revlimid untuk dikonsumsi
Sebelum memulai perawatan, dokter Anda akan memberi tahu Anda:
- dosis Revlimid yang harus diminum
- dosis obat lain yang akan dikonsumsi bersamaan dengan Revlimid, jika diresepkan
- pada hari mana dari siklus pengobatan untuk mengambil setiap obat.
Dokter mungkin mengamati perubahan pada kulit, seperti bintik merah atau ruam.
Dokter Anda mungkin juga memutuskan untuk mengubah dosis Revlimid atau obat lain selama perawatan, berdasarkan hasil tes darah dan kondisi umum Anda (lihat bagian 2, "Apa yang perlu Anda ketahui sebelum menggunakan Revlimid").
Bagaimana dan kapan harus menggunakan Revlimid
- Kapsul harus ditelan utuh, sebaiknya dengan air.
- Jangan merusak, membuka atau mengunyah kapsul.
- Kapsul dapat diminum dengan atau tanpa makanan.
- Anda harus menggunakan Revlimid pada hari-hari yang ditentukan pada waktu yang hampir bersamaan.
Untuk mengeluarkan kapsul dari blister, tekan salah satu sisi kapsul saja, dorong melalui aluminium foil, jangan menekan bagian tengah kapsul, jika tidak bisa pecah.
Durasi pengobatan dengan Revlimid
Revlimid diambil dalam siklus pengobatan, masing-masing berlangsung selama 28 hari (lihat 'Siklus pengobatan' di atas). Anda harus melanjutkan pengobatan sampai dokter Anda memberitahu Anda untuk menghentikan pengobatan.
Jika Anda lupa minum Revlimid
Jika Anda lupa mengambil Revlimid pada waktu yang biasa e
- kurang dari 12 jam telah berlalu: segera minum kapsul Anda
- lebih dari 12 jam telah berlalu: jangan minum kapsul yang terlupakan, tetapi minum kapsul berikutnya keesokan harinya pada waktu yang biasa.
Jika Anda memiliki pertanyaan lebih lanjut tentang penggunaan obat ini, tanyakan kepada dokter atau apoteker Anda.
Overdosis Apa yang harus dilakukan jika Anda terlalu banyak mengonsumsi Revlimid
Jika Anda telah menggunakan Revlimid lebih dari yang diperintahkan, segera beri tahu dokter Anda.
Efek Samping Apa efek samping Revlimid?
Seperti semua obat-obatan, obat ini dapat menyebabkan efek samping, meskipun tidak semua orang mendapatkannya.
Efek samping serius yang dapat mempengaruhi lebih dari 1 dari 10 orang
Revlimid dapat mengurangi jumlah sel darah putih yang melawan infeksi dan sel darah yang meningkatkan pembekuan darah (trombosit), yang dapat menyebabkan gangguan perdarahan, misalnya. mimisan dan memar. Revlimid juga dapat menyebabkan pembekuan darah di pembuluh darah (trombosis).
Oleh karena itu, Anda harus segera mencari pertolongan medis jika Anda mengalami salah satu dari efek samping berikut:
- demam, menggigil, sakit tenggorokan, batuk, sariawan atau gejala infeksi lainnya (termasuk di dalam aliran darah (sepsis))
- pendarahan atau memar tanpa adanya luka
- nyeri di dada atau kaki
- sesak napas.
Jika Anda mengalami salah satu dari efek samping yang tercantum di atas, segera beri tahu dokter Anda.
Efek samping lainnya tercantum di bawah ini
Penting untuk dicatat bahwa sejumlah kecil pasien dapat mengembangkan jenis kanker lain dan ada kemungkinan bahwa risiko ini dapat meningkat dengan pengobatan dengan Revlimid; oleh karena itu, dokter Anda harus hati-hati mempertimbangkan manfaat dan risiko saat meresepkan Revlimid untuk Anda.
Efek samping yang sangat umum dapat mempengaruhi lebih dari 1 dari 10 orang:
- Penurunan jumlah sel darah merah (anemia), yang dapat menyebabkan kelelahan dan kelemahan
- Sembelit, diare, mual, kulit kemerahan, ruam, muntah, kram otot, nyeri otot, nyeri tulang, nyeri sendi, kelelahan, pembengkakan umum, termasuk pembengkakan pada lengan dan kaki
- Gejala demam dan flu, termasuk demam, nyeri otot, sakit kepala, sakit telinga, dan kedinginan
- Mati rasa, kesemutan atau sensasi terbakar pada kulit, nyeri pada tangan atau kaki, pusing, tremor, perubahan rasa
- Nyeri dada menjalar ke lengan, leher, rahang, punggung atau perut, dengan sensasi berkeringat dan sesak napas, mual atau muntah, yang mungkin merupakan gejala serangan jantung (infark miokard)
- Pengurangan nafsu makan
- Rendahnya kadar kalium dalam darah
- Nyeri kaki (yang mungkin merupakan gejala trombosis), nyeri dada atau sesak napas (yang mungkin merupakan gejala pembekuan darah di paru-paru, yang disebut emboli paru)
- Infeksi apapun
- Infeksi paru-paru dan saluran pernapasan bagian atas, sesak napas
- Penglihatan kabur
- Penglihatan kabur (katarak)
- Masalah ginjal
- Perubahan protein dalam darah yang dapat menyebabkan pembengkakan arteri (vaskulitis)
- Peningkatan gula darah (diabetes)
- Sakit kepala
- Kulit kering
- Sakit perut
- Perubahan mood, sulit tidur
Efek samping yang umum dapat mempengaruhi hingga 1 dari 10 orang:
- Infeksi pada sinus di sekitar hidung
- Pendarahan dari gusi, perut atau usus
- Peningkatan rasa sakit, ukuran tumor, kemerahan di sekitar tumor
- Peningkatan atau penurunan tekanan darah, detak jantung yang lambat, cepat atau tidak teratur
- Menggelapkan kulit
- Ruam, kulit pecah-pecah, terkelupas atau terkelupas
- Gatal-gatal, gatal-gatal, peningkatan keringat, dehidrasi
- Sakit mulut dengan bisul, mulut kering, kesulitan menelan
- Sakit perut
- Produksi urin jauh lebih banyak atau lebih sedikit dari biasanya (yang mungkin merupakan gejala gagal ginjal), darah dalam urin
- Sesak napas, terutama saat berbaring (yang bisa menjadi gejala gagal jantung)
- Kesulitan mendapatkan ereksi
- Stroke, pingsan
- Kelemahan otot
- Pembengkakan sendi
- Perubahan hormon tiroid dalam darah, rendahnya kadar kalsium, fosfat atau magnesium dalam darah
- Depresi
- Ketulian
- Tes fungsi hati yang tidak normal
- Gangguan keseimbangan, kesulitan gerakan
- Telinga berdenging (tinnitus)
- Kelebihan zat besi
- Haus
- Kebingungan
- Sakit gigi
- Penurunan berat badan.
Efek samping yang tidak umum dapat mempengaruhi hingga 1 dari 100 orang:
- Perdarahan di dalam tengkorak
- Masalah peredaran darah
- Kehilangan penglihatan
- Hilangnya gairah seks (libido)
- Aliran urin yang melimpah disertai nyeri dan kelemahan pada tulang, yang bisa jadi merupakan gejala gangguan ginjal (sindrom Fanconi)
- Sakit perut, kembung atau diare, yang mungkin merupakan gejala radang usus besar (disebut kolitis atau tiflitis)
- Produksi urin lebih banyak atau lebih sedikit dari biasanya, yang mungkin merupakan gejala dari jenis masalah ginjal (disebut nekrosis tubulus ginjal).
- Perubahan warna kulit, kepekaan terhadap sinar matahari
- Beberapa jenis kanker kulit
- Gatal-gatal, ruam, pembengkakan mata, mulut atau wajah, kesulitan bernapas atau gatal-gatal, yang mungkin merupakan gejala reaksi alergi.
Efek samping yang jarang dapat mempengaruhi hingga 1 dari 1.000 orang:
- Reaksi alergi parah, yang mungkin dimulai sebagai ruam di satu area tetapi menyebar dengan kehilangan kulit yang luas di seluruh tubuh (sindrom Stevens-Johnson dan / atau nekrolisis epidermal toksik).
- Sindrom lisis tumor - komplikasi metabolik yang dapat terjadi selama pengobatan tumor dan kadang-kadang bahkan tanpa pengobatan. Komplikasi ini disebabkan oleh produk pemecahan sel kanker yang sekarat dan dapat mencakup komplikasi berikut: perubahan parameter hematologis; nilai tinggi kalium, fosfor, dan asam urat; dan nilai kalsium rendah yang akibatnya menyebabkan perubahan fungsi ginjal, detak jantung, kejang dan, terkadang, kematian.
Frekuensi tidak diketahui: frekuensi tidak dapat diperkirakan dari data yang tersedia:
- Nyeri yang tiba-tiba atau ringan tetapi memburuk di perut bagian atas dan/atau punggung yang berlangsung selama beberapa hari, mungkin disertai mual, muntah, demam, dan denyut nadi yang cepat. Gejala-gejala ini mungkin disebabkan oleh peradangan pankreas.
- Mengi, sesak napas, atau batuk kering, yang bisa jadi merupakan gejala yang disebabkan oleh peradangan pada jaringan paru-paru.
- Perubahan warna kekuningan pada kulit, selaput lendir atau mata (jaundice), tinja berwarna terang, urin berwarna gelap, kulit gatal, ruam, nyeri atau pembengkakan pada perut. Ini bisa menjadi gejala kerusakan hati (penyakit hati).
- Kasus kerusakan otot yang jarang (nyeri, kelemahan atau pembengkakan otot), yang dapat menyebabkan masalah ginjal (rhabdomyolysis), telah diamati, beberapa di antaranya ketika Revlimid diberikan dengan statin (sejenis obat penurun kolesterol).
- Penyakit yang menyerang kulit dan disebabkan oleh peradangan pembuluh darah kecil, disertai nyeri pada persendian dan demam (leukocytoclastic vasculitis).
- Kerusakan lambung atau dinding usus, yang dapat menyebabkan infeksi yang sangat serius.Beri tahu dokter Anda jika Anda mengalami sakit perut yang parah, demam, mual, muntah, darah dalam tinja, atau perubahan kebiasaan buang air besar.
Pelaporan efek samping
Jika Anda mendapatkan efek samping, bicarakan dengan dokter, apoteker atau perawat Anda. Ini termasuk kemungkinan efek samping yang tidak tercantum dalam selebaran ini. Anda juga dapat melaporkan efek samping secara langsung melalui sistem pelaporan nasional yang tercantum dalam Lampiran V. efek samping yang dapat Anda bantu memberikan informasi lebih lanjut tentang keamanan obat ini.
Kadaluwarsa dan Retensi
- Jauhkan obat ini dari pandangan dan jangkauan anak-anak.
- Jangan menggunakan obat ini setelah tanggal kadaluwarsa yang tertera pada blister dan karton setelah "EXP". Tanggal kedaluwarsa mengacu pada hari terakhir bulan itu.
- Obat ini tidak memerlukan kondisi penyimpanan khusus.
- Jangan gunakan obat ini jika Anda melihat kemasan yang rusak atau menunjukkan tanda-tanda kerusakan.
- Jangan membuang obat apa pun melalui air limbah atau limbah rumah tangga. Tanyakan apoteker Anda bagaimana cara membuang obat yang sudah tidak digunakan lagi. Ini akan membantu melindungi lingkungan.
Batas waktu "> Informasi lainnya
Apa isi Revlimid?
Revlimid 2.5 mg kapsul keras:
- Bahan aktifnya adalah lenalidomide. Setiap kapsul mengandung 2,5 mg lenalidomide.
- Bahan-bahan lainnya adalah:
- isi kapsul: laktosa anhidrat, selulosa mikrokristalin, natrium kroskarmelosa dan magnesium stearat
- cangkang kapsul: gelatin, titanium dioksida (E171), nila carmine (E132) dan oksida besi kuning (E172)
- tinta huruf: lak, propilen glikol, kalium hidroksida dan oksida besi hitam (E172).
Revlimid kapsul keras 5 mg:
- Bahan aktifnya adalah lenalidomide. Tiap kapsul mengandung 5 mg lenalidomide.
- Bahan-bahan lainnya adalah:
- isi kapsul: laktosa anhidrat, selulosa mikrokristalin, natrium kroskarmelosa dan magnesium stearat
- cangkang kapsul: gelatin dan titanium dioksida (E171)
- tinta huruf: lak, propilen glikol, kalium hidroksida dan oksida besi hitam (E172).
Revlimid 7,5 mg kapsul keras:
- Bahan aktifnya adalah lenalidomide. Setiap kapsul mengandung 7,5 mg lenalidomide.
- Bahan-bahan lainnya adalah:
- isi kapsul: laktosa anhidrat, selulosa mikrokristalin, natrium kroskarmelosa dan magnesium stearat
- cangkang kapsul: gelatin, titanium dioksida (E171), oksida besi kuning (E172)
- tinta huruf: lak, propilen glikol, kalium hidroksida dan oksida besi hitam (E172).
Revlimid 10 mg kapsul keras:
- Bahan aktifnya adalah lenalidomide. Tiap kapsul mengandung 10 mg lenalidomide.
- Bahan-bahan lainnya adalah:
- isi kapsul: laktosa anhidrat, selulosa mikrokristalin, natrium kroskarmelosa dan magnesium stearat
- sediaan kapsul: gelatin, titanium dioksida (E171), nila carmine (E132) dan oksida besi kuning (E172)
- tinta huruf: lak, propilen glikol, kalium hidroksida dan oksida besi hitam (E172).
Revlimid 15 mg kapsul keras:
- Bahan aktifnya adalah lenalidomide. Tiap kapsul mengandung lenalidomide 15 mg.
- Bahan-bahan lainnya adalah:
- isi kapsul: laktosa anhidrat, selulosa mikrokristalin, natrium kroskarmelosa dan magnesium stearat
- cangkang kapsul: gelatin, titanium dioksida (E171) dan nila carmine (E132)
- tinta huruf: lak, propilen glikol, kalium hidroksida dan oksida besi hitam (E172).
Revlimid 20 mg kapsul keras:
- Bahan aktifnya adalah lenalidomide. Tiap kapsul mengandung lenalidomide 20 mg.
- Bahan-bahan lainnya adalah:
- isi kapsul: laktosa anhidrat, selulosa mikrokristalin, natrium kroskarmelosa dan magnesium stearat
- cangkang kapsul: gelatin, titanium dioksida (E171), nila carmine (E132) dan oksida besi kuning (E172)
- tinta huruf: lak, propilen glikol, kalium hidroksida dan oksida besi hitam (E172).
Revlimid 25 mg kapsul keras:
- Bahan aktifnya adalah lenalidomide. Tiap kapsul mengandung lenalidomide 25 mg.
- Bahan-bahan lainnya adalah:
- isi kapsul: laktosa anhidrat, selulosa mikrokristalin, natrium kroskarmelosa dan magnesium stearat
- cangkang kapsul: gelatin dan titanium dioksida (E171)
- tinta huruf: lak, propilen glikol, kalium hidroksida dan oksida besi hitam (E172).
Seperti apa Revlimid dan isi paketnya
Kapsul keras Revlimid 2.5 mg berwarna biru-hijau/putih, bertanda "REV 2.5 mg".
Kapsul disediakan dalam kemasan, masing-masing berisi satu atau tiga lepuh. Setiap blister berisi tujuh kapsul, dengan total 7 atau 21 kapsul per bungkus.
Kapsul keras Revlimid 5 mg berwarna putih, bertanda "REV 5 mg".
Kapsul disediakan dalam kemasan, masing-masing berisi satu atau tiga lepuh. Setiap blister berisi tujuh kapsul, dengan total 7 atau 21 kapsul per bungkus.
Kapsul keras Revlimid 7,5 mg berwarna kuning pucat/putih, bertanda "REV 7,5 mg".
Kapsul disediakan dalam kemasan, masing-masing berisi tiga lepuh. Setiap blister berisi tujuh kapsul, dengan total 21 kapsul per bungkus.
Kapsul keras Revlimid 10 mg berwarna biru-hijau/kuning muda, bertanda "REV 10 mg".
Kapsul disediakan dalam kemasan, masing-masing berisi tiga lepuh. Setiap blister berisi tujuh kapsul, dengan total 21 kapsul per bungkus.
Kapsul keras Revlimid 15 mg berwarna biru muda/putih, bertanda "REV 15 mg".
Kapsul disediakan dalam kemasan, masing-masing berisi tiga lepuh. Setiap blister berisi tujuh kapsul, dengan total 21 kapsul per bungkus.
Revlimid kapsul keras 20 mg berwarna biru-hijau/biru muda, bertanda "REV 20 mg".
Kapsul disediakan dalam kemasan, masing-masing berisi tiga lepuh. Setiap blister berisi tujuh kapsul, dengan total 21 kapsul per bungkus.
Kapsul keras Revlimid 25 mg berwarna putih, bertanda "REV 25 mg".
Kapsul disediakan dalam kemasan, masing-masing berisi tiga lepuh. Setiap blister berisi tujuh kapsul, dengan total 21 kapsul per bungkus.
Sumber Paket Leaflet: AIFA (Badan Obat Italia). Konten yang diterbitkan pada Januari 2016. Informasi yang ada mungkin tidak up-to-date.
Untuk memiliki akses ke versi terbaru, disarankan untuk mengakses situs web AIFA (Badan Obat Italia). Penafian dan informasi yang berguna.
01.0 NAMA PRODUK OBAT -
REVLIMID 10 MG KAPSUL KERAS
Produk obat tunduk pada pemantauan tambahan. Ini akan memungkinkan identifikasi cepat informasi keselamatan baru. Profesional perawatan kesehatan diminta untuk melaporkan setiap dugaan reaksi merugikan. Lihat bagian 4.8 untuk informasi tentang cara melaporkan reaksi merugikan.
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF -
Tiap kapsul mengandung 10 mg lenalidomide.
Eksipien dengan efek yang diketahui:
Setiap kapsul mengandung 294 mg laktosa anhidrat.
Untuk daftar lengkap eksipien, lihat bagian 6.1.
03.0 FORMULIR FARMASI -
Kapsul keras.
Kapsul biru-hijau / kuning muda, ukuran 0,21,7 mm, bertanda "REV 10 mg".
04.0 INFORMASI KLINIS -
04.1 Indikasi Terapi -
Mieloma multipel
Revlimid diindikasikan untuk pengobatan pasien dewasa dengan multiple myeloma yang sebelumnya tidak diobati yang tidak memenuhi syarat untuk transplantasi (lihat bagian 4.2).
Revlimid, dalam kombinasi dengan deksametason, diindikasikan untuk pengobatan pasien dewasa dengan multiple myeloma yang telah menerima setidaknya satu terapi sebelumnya.
Sindrom mielodisplastik
Revlimid diindikasikan untuk pengobatan pasien dengan anemia tergantung transfusi karena sindrom myelodysplastic risiko rendah atau menengah-1 (MDS) yang terkait dengan kelainan sitogenetik penghapusan 5q terisolasi, ketika pilihan pengobatan lain tidak mencukupi atau tidak memadai.
Limfoma sel mantel
Revlimid diindikasikan untuk pengobatan pasien dewasa dengan limfoma sel mantel yang kambuh atau refrakter (lihat bagian 4.4 dan 5.1).
04.2 Posologi dan cara pemberian -
Pengobatan dengan Revlimid harus diawasi oleh dokter yang berpengalaman dalam penggunaan terapi kanker (lihat bagian 4.4, kariotipe).
Dosis
Multiple myeloma yang baru didiagnosis
Lenalidomide dalam kombinasi dengan deksametason sampai perkembangan penyakit, pada non-pasien memenuhi syarat untuk transplantasi
Pengobatan dengan lenalidomide tidak boleh dimulai jika jumlah neutrofil absolut (Mutlak
Jumlah Neutrofil, ANC) adalah
Dosis yang direkomendasikan
Dosis awal lenalidomide yang direkomendasikan adalah 25 mg per oral sekali sehari pada hari ke 1-21 dari siklus 28 hari yang berulang. Dosis deksametason yang dianjurkan adalah 40 mg per oral sekali sehari pada hari ke 1, 8, 15, dan 22 dari siklus 28 hari yang berulang. Pasien dapat melanjutkan terapi lenalidomide dan deksametason sampai perkembangan penyakit atau intoleransi berkembang.
Dosis dapat dilanjutkan atau dimodifikasi berdasarkan temuan klinis dan laboratorium (lihat bagian 4.4). Untuk pasien 75 tahun, dosis awal deksametason adalah 20 mg / hari pada hari 1, 8, 15 dan 22 dari setiap siklus pengobatan 28 hari. Dosis lenalidomide yang dianjurkan untuk pasien dengan gangguan ginjal sedang adalah 10 mg sekali sehari.
Penyesuaian dosis yang direkomendasikan selama pengobatan dan setelah dimulainya kembali pengobatan
Seperti yang dirangkum dalam tabel di bawah, penyesuaian dosis direkomendasikan untuk pengelolaan trombositopenia dan neutropenia Grade 3 atau 4, atau untuk pengelolaan toksisitas Grade 3 atau 4 lainnya yang diyakini terkait dengan lenalidomide.
• Tingkat pengurangan dosis
• Trombositopenia
a Jika terjadi toksisitas yang membatasi dosis (Toksisitas Pembatas Dosis, DLT)> Hari ke 15 siklus, dosis lenalidomide akan dihentikan setidaknya selama sisa siklus 28 hari saat ini.
• Neutropenia
Dalam kasus neutropenia, dokter harus mempertimbangkan penggunaan faktor pertumbuhan dalam manajemen pasien.
Jika dosis lenalidomide telah dikurangi karena DLT hematologis, dosis lenalidomide dapat diperkenalkan kembali pada tingkat dosis yang lebih tinggi berikutnya (sampai dosis awal), atas kebijaksanaan dokter yang merawat, jika terapi lenalidomide / deksametason dilanjutkan menghasilkan sumsum tulang yang lebih baik. fungsi (tidak adanya DLT untuk setidaknya 2 siklus berturut-turut dan ANC 1.500 / mcl, dengan jumlah trombosit 100.000 / mcl, pada awal siklus baru pada dosis saat ini).
Lenalidomide dalam kombinasi dengan melphalan dan prednison, diikuti dengan monoterapi pemeliharaan, di pasien yang tidak memenuhi syarat untuk transplantasi
Pengobatan lenalidomide tidak boleh dimulai jika ANC tidak
Dosis yang direkomendasikan
Dosis awal yang dianjurkan adalah lenalidomide 10 mg/hari per oral pada hari ke 1-21 dari siklus 28 hari berulang hingga 9 siklus, melphalan 0,18 mg/kg per oral pada hari ke 1-4 dari siklus berulang 28 hari, prednison 2 mg/ kg secara oral pada hari 1-4 dari siklus 28 hari yang berulang. Pasien menyelesaikan 9 siklus atau tidak dapat menyelesaikan terapi kombinasi karena intoleransi harus diperlakukan dengan monoterapi lenalidomide, 10 mg / hari secara oral, pada hari 1-21 dari siklus berulang, 28 hari sampai perkembangan penyakit. Dosis dapat dilanjutkan atau dimodifikasi berdasarkan temuan klinis dan laboratorium (lihat bagian 4.4).
Penyesuaian dosis yang direkomendasikan selama pengobatan dan setelah dimulainya kembali pengobatan
Seperti yang dirangkum dalam tabel di bawah, penyesuaian dosis direkomendasikan untuk pengobatan trombositopenia atau neutropenia Grade 3 atau 4, atau untuk pengelolaan toksisitas Grade 3 atau 4 lainnya yang dianggap terkait dengan lenalidomide.
• Tingkat pengurangan dosis
Jika neutropenia adalah satu-satunya toksisitas pada dosis apapun, tambahkan faktor perangsang koloni granulosit (G-CSF) dan pertahankan dosis lenalidomide..
• Trombositopenia
• Neutropenia
a Jika subjek belum menerima terapi G-CSF, mulai terapi G-CSF. Pada Hari 1 siklus berikutnya, lanjutkan GCSF sesuai kebutuhan dan pertahankan dosis melphalan jika neutropenia adalah satu-satunya DLT. Jika tidak, kurangi satu tingkat dosis pada awal siklus berikutnya.
Dalam kasus neutropenia, penggunaan faktor pertumbuhan dalam manajemen pasien harus dipertimbangkan.
Multiple myeloma dengan setidaknya satu terapi sebelumnya
Dosis yang direkomendasikan
Dosis awal yang dianjurkan adalah 25 mg lenalidomide secara oral sekali sehari pada hari ke 1-21 dari siklus 28 hari yang berulang. Dosis deksametason yang dianjurkan adalah 40 mg per oral sekali sehari pada hari 1-4, 9-12 dan 17-20 setiap siklus 28 hari untuk 4 siklus pertama terapi dan 40 mg sekali sehari setelahnya. setiap 28 hari.
Dosis dapat dilanjutkan atau dimodifikasi berdasarkan temuan klinis dan laboratorium (lihat bagian 4.4). Dokter harus hati-hati mengevaluasi dosis deksametason untuk digunakan, dengan mempertimbangkan kondisi pasien dan status penyakit.
Pengobatan dengan lenalidomide tidak boleh dimulai jika ANC adalah sumsum tulang oleh sel plasma, jika jumlah trombositnya
Penyesuaian dosis yang direkomendasikan selama pengobatan dan setelah dimulainya kembali pengobatan
Seperti dirangkum dalam tabel di bawah, penyesuaian dosis direkomendasikan untuk pengobatan neutropenia atau trombositopenia tingkat 3 atau 4, atau untuk pengelolaan toksisitas tingkat 3 atau 4 yang dianggap terkait dengan lenalidomide.
• Tingkat pengurangan dosis
• Trombositopenia
• Neutropenia
Dalam kasus neutropenia, penggunaan faktor pertumbuhan dalam manajemen pasien harus dipertimbangkan.
Sindrom mielodisplastik
Pengobatan lenalidomide tidak boleh dimulai jika ANC tidak
Dosis yang direkomendasikan
Dosis awal yang dianjurkan adalah 10 mg lenalidomide secara oral sekali sehari pada hari ke 1-21 dari siklus 28 hari yang berulang. Dosis dapat dilanjutkan atau dimodifikasi berdasarkan temuan klinis dan laboratorium (lihat bagian 4.4).
Penyesuaian dosis yang direkomendasikan selama pengobatan dan setelah dimulainya kembali pengobatan
Seperti dirangkum dalam tabel di bawah, penyesuaian dosis direkomendasikan untuk pengobatan neutropenia atau trombositopenia tingkat 3 atau 4, atau untuk pengelolaan toksisitas tingkat 3 atau 4 yang dianggap terkait dengan lenalidomide.
• Tingkat pengurangan dosis
Untuk pasien yang memulai dengan dosis 10 mg dan mengalami trombositopenia atau neutropenia:
• Trombositopenia
• Neutropenia
Suspensi lenalidomide
Pasien yang tidak memiliki respon eritroid ringan dalam waktu 4 bulan setelah memulai terapi, ditunjukkan dengan pengurangan setidaknya 50% dalam kebutuhan transfusi atau, jika tidak menerima transfusi, dengan peningkatan hemoglobin 1 g / dl, harus menghentikan lenalidomide. perlakuan.
Limfoma sel mantel
Dosis yang direkomendasikan
Dosis awal yang dianjurkan adalah 25 mg lenalidomide secara oral sekali sehari pada hari ke 1-21 dari siklus 28 hari yang berulang.
Pengujian dilanjutkan atau dimodifikasi berdasarkan temuan klinis dan laboratorium (lihat bagian 4.4).
Penyesuaian dosis yang direkomendasikan selama pengobatan dan setelah dimulainya kembali pengobatan
Seperti dirangkum dalam tabel di bawah, penyesuaian dosis direkomendasikan untuk pengobatan neutropenia atau trombositopenia Tingkat 3 atau 4, atau untuk pengelolaan toksisitas Tingkat 3 atau 4 yang dianggap terkait dengan lenalidomide.
• Tingkat pengurangan dosis
1 - Di negara-negara di mana kapsul 2,5 mg tersedia.
• Trombositopenia
• Neutropenia
• Reaksi suar tumor
Pengobatan dengan lenalidomide dapat dilanjutkan pada pasien dengan Reaksi Flare Tumor, Ganti rugi pesangon tingkat 1 atau 2, tanpa interupsi atau modifikasi, atas kebijaksanaan dokter. Pada pasien dengan TFR Grade 3 atau 4, pengobatan lenalidomide harus dihentikan sampai TFR diturunkan menjadi Grade 1; Untuk manajemen gejala, pasien dapat diobati sesuai dengan pedoman TFR grade 1 dan 2 (lihat bagian 4.4).
Semua pasien
Untuk efek toksik Tingkat 3 atau 4 lainnya yang diyakini terkait dengan lenalidomide, pengobatan harus dihentikan dan dilanjutkan dengan dosis yang lebih rendah berikutnya hanya jika toksisitas telah menurun menjadi Tingkat 2 atas kebijaksanaan dokter.
Penghentian atau penghentian lenalidomide harus dipertimbangkan dalam kasus ruam kulit tingkat 2 atau 3. Pengobatan dengan lenalidomide harus dihentikan dalam kasus angioedema, ruam tingkat 4, ruam eksfoliatif atau bulosa, atau jika dicurigai Stevens-Johnson (SSJ) atau epidermal toksik nekrolisis (NET), dan tidak boleh dilanjutkan setelah penghentian karena reaksi ini.
populasi khusus
Populasi pediatrik
Revlimid tidak boleh digunakan pada anak-anak dan remaja sejak lahir hingga usia 18 tahun karena masalah keamanan (lihat bagian 4.4).
pasien lanjut usia
Data farmakokinetik yang tersedia saat ini dijelaskan di bagian 5.2. Lenalidomide telah digunakan dalam studi klinis pada pasien dengan multiple myeloma hingga usia 91 tahun, pada pasien dengan sindrom myelodysplastic hingga usia 95 tahun dan pada pasien dengan limfoma sel mantel hingga usia 88 tahun (lihat bagian 5.1).
Pada pasien multiple myeloma yang baru didiagnosis berusia 75 tahun dan lebih tua yang diobati dengan lenalidomide, terdapat insiden yang lebih tinggi dari reaksi merugikan yang serius dan reaksi merugikan yang menyebabkan penghentian pengobatan (lihat bagian 4.4) Pasien multiple myeloma yang baru didiagnosis berusia 75 tahun atau lebih harus hati-hati dievaluasi sebelum mempertimbangkan pengobatan (lihat bagian 4.4).
• Mieloma multipel yang baru didiagnosis
Untuk pasien di atas 75 tahun yang diobati dengan lenalidomide dalam kombinasi dengan deksametason, dosis awal deksametason adalah 20 mg / hari pada hari 1, 8, 15 dan 22 dari setiap siklus pengobatan 28 hari.
Tidak ada penyesuaian dosis yang diusulkan untuk pasien di atas 75 tahun yang diobati dengan lenalidomide dalam kombinasi dengan melphalan dan prednison.
Dalam uji klinis dari multiple myeloma yang baru didiagnosis pada pasien yang tidak memenuhi syarat transplantasi, terapi kombinasi lenalidomide kurang ditoleransi pada pasien di atas 75 tahun dibandingkan pada populasi yang lebih muda. Di antara pasien ini, persentase yang menghentikan pengobatan karena intoleransi (efek samping tingkat 3 atau 4 dan efek samping yang serius) lebih tinggi daripada pasien berusia
• Multiple myeloma yang sebelumnya diobati dengan setidaknya satu terapi
Persentase penderita multiple myeloma berusia 65 tahun atau lebih tidak berbeda nyata antara kelompok lenalidomide/dexamethasone dan placebo/dexamethasone. Secara umum, tidak ada perbedaan dalam keamanan dan kemanjuran yang diamati antara pasien ini dan pasien yang lebih muda, meskipun kecenderungan yang lebih besar dari pasien yang lebih tua tidak dapat dikesampingkan.
• Sindrom mielodisplastik
Untuk pasien dengan sindrom myelodysplastic yang diobati dengan lenalidomide, tidak ada perbedaan keseluruhan dalam keamanan dan kemanjuran yang diamati antara pasien berusia di atas 65 tahun dan pasien yang lebih muda.
• Limfoma sel mantel
Untuk pasien dengan limfoma sel mantel yang diobati dengan lenalidomide, tidak ada perbedaan keseluruhan dalam keamanan dan kemanjuran yang diamati antara pasien berusia 65 tahun ke atas dan pasien berusia di bawah 65 tahun.
Karena pasien lanjut usia lebih mungkin mengalami gangguan fungsi ginjal, perhatian khusus harus diberikan dalam pemilihan dosis dan pemantauan fungsi ginjal harus dilakukan sebagai tindakan pencegahan.
Pasien dengan insufisiensi ginjal
Lenalidomide secara substansial diekskresikan melalui ginjal; pada pasien dengan derajat insufisiensi ginjal yang lebih tinggi, tolerabilitas pengobatan dapat diubah (lihat bagian 4.4). Perhatian khusus harus diberikan dalam memilih dosis dan pemantauan fungsi ginjal dianjurkan.
Tidak ada penyesuaian dosis yang diperlukan pada pasien dengan insufisiensi ginjal ringan dan multiple myeloma, sindrom myelodysplastic atau limfoma sel mantel. Pada pasien dengan insufisiensi ginjal sedang atau berat atau penyakit ginjal stadium akhir, pada awal terapi dan selama pengobatan, penyesuaian dosis berikut direkomendasikan.Tidak ada pengalaman uji klinis fase III pada pasien dengan Penyakit Ginjal Tahap Akhir (ESRD). ) (dialisis CLcr).
• Mieloma multipel
1 Dosis dapat ditingkatkan menjadi 15 mg sekali sehari setelah 2 siklus jika pasien tidak merespon pengobatan tetapi mentoleransi obat.
2 Di negara-negara di mana kapsul 7,5 mg tersedia.
• Sindrom mielodisplastik
* Tingkat pengurangan dosis yang direkomendasikan selama pengobatan dan setelah dimulainya kembali pengobatan, untuk mengelola neutropenia atau trombositopenia tingkat 3 atau 4, atau toksisitas tingkat 3 atau 4 lainnya yang dianggap terkait dengan lenalidomide, seperti dijelaskan di atas.
• Limfoma sel mantel
1 Dosis dapat ditingkatkan menjadi 15 mg sekali sehari setelah 2 siklus jika pasien tidak merespon pengobatan tetapi mentoleransi obat.
2 Di negara-negara di mana kapsul 7,5 mg tersedia.
Setelah memulai terapi lenalidomide, modifikasi dosis lenalidomide berikutnya pada pasien dengan gangguan fungsi ginjal harus didasarkan pada tolerabilitas pengobatan untuk pasien individu, seperti dijelaskan di atas.
Pasien dengan gangguan hati
Lenalidomide belum dipelajari secara formal pada pasien dengan gangguan hati dan tidak ada rekomendasi dosis khusus.
Cara pemberian
Penggunaan lisan.
Kapsul Revlimid harus diminum pada hari yang ditentukan, sekitar waktu yang sama. Kapsul tidak boleh dibuka, dipecah atau dikunyah. Kapsul harus ditelan utuh, sebaiknya dengan air, dengan atau tanpa makanan. Pasien dapat mengambil dosis yang terlewat jika kurang dari 12 jam setelah waktu yang dijadwalkan, sebaliknya jika lebih dari 12 jam, pasien tidak boleh mengambil dosis yang terlewat, tetapi menunggu dosis yang biasa. waktu hari berikutnya untuk mengambil dosis berikutnya.
Disarankan untuk memberikan tekanan hanya pada satu sisi kapsul untuk mengeluarkannya dari lepuh, sehingga mengurangi risiko deformasi atau pecahnya kapsul.
04.3 Kontraindikasi -
• Hipersensitivitas terhadap zat aktif atau salah satu eksipien yang tercantum di bagian 6.1.
• Wanita hamil.
• Wanita yang berpotensi melahirkan anak, kecuali semua kondisi Program Pencegahan Kehamilan terpenuhi (lihat bagian 4.4 dan 4.6).
04.4 Peringatan khusus dan tindakan pencegahan yang tepat untuk digunakan -
Tindakan pencegahan dalam kasus kehamilan
Lenalidomide secara struktural terkait dengan thalidomide, zat aktif dengan efek teratogenik yang diketahui pada manusia, yang menyebabkan cacat lahir parah yang mengancam jiwa. Lenalidomide menyebabkan malformasi pada monyet mirip dengan yang dijelaskan untuk thalidomide (lihat bagian 4.6 dan 5.3). diharapkan pada manusia selama kehamilan.
Kondisi Program Pencegahan Kehamilan harus dipenuhi untuk semua pasien, kecuali ada bukti kuat bahwa pasien tidak dapat hamil.
Kriteria untuk menetapkan bahwa seorang wanita tidak berpotensi melahirkan anak
Seorang pasien wanita atau pasangan pasien pria dianggap mampu untuk hamil kecuali dia memenuhi setidaknya satu dari kriteria berikut:
• Usia 50 tahun dan amenore alami * selama 1 tahun
• Kegagalan ovarium prematur dikonfirmasi oleh ginekolog
• Salpingo-ooforektomi bilateral atau histerektomi sebelumnya
• Genotipe XY, sindrom Turner, agenesis uterus.
* Amenore setelah terapi antikanker atau selama menyusui tidak mengesampingkan potensi kesuburan.
Orientasi
Lenalidomide dikontraindikasikan untuk wanita yang berpotensi melahirkan anak kecuali semua kondisi berikut terpenuhi:
• Pasien menyadari bahwa risiko teratogenik pada janin diperkirakan terjadi
• Pasien menyadari perlunya menggunakan metode kontrasepsi yang efektif, tanpa gangguan, 4 minggu sebelum memulai pengobatan, selama pengobatan dan hingga 4 minggu setelah pengobatan berakhir.
• Bahkan dengan adanya amenore, pasien yang berpotensi melahirkan anak harus mengikuti semua rekomendasi untuk kontrasepsi yang efektif
• Pasien harus mampu mematuhi tindakan kontrasepsi yang efektif
• Pasien diberi tahu dan sadar akan konsekuensi potensial dari kehamilan dan kebutuhan untuk mencari pertolongan medis segera jika ada risiko kehamilan
• Pasien menyadari perlunya memulai pengobatan segera setelah lenalidomide diberikan setelah tes kehamilan negatif
• Pasien sadar akan kebutuhan dan setuju untuk menjalani tes kehamilan setiap 4 minggu, kecuali dalam kasus sterilisasi yang dikonfirmasi dengan ligasi tuba
• Pasien mengakui bahwa dia menyadari risiko dan tindakan pencegahan yang diperlukan terkait dengan penggunaan lenalidomide
Untuk pasien laki-laki yang memakai lenalidomide, studi farmakokinetik telah menunjukkan bahwa, selama pengobatan, lenalidomide hadir pada tingkat yang sangat rendah dalam air mani dan tidak terdeteksi dalam air mani subyek sehat 3 hari setelah penghentian zat ( lihat paragraf 5.2). Sebagai tindakan pencegahan, semua pasien pria yang menggunakan lenalidomide harus memenuhi ketentuan berikut:
• Waspadai risiko teratogenik yang diharapkan jika terjadi aktivitas seksual dengan wanita yang sedang hamil atau yang berpotensi melahirkan anak
• Sadar akan kebutuhan untuk menggunakan kondom jika melakukan aktivitas seksual dengan wanita hamil atau berpotensi subur yang tidak menggunakan kontrasepsi yang efektif (bahkan jika pria tersebut telah menjalani vasektomi) selama pengobatan dan selama 1 minggu setelah penangguhan dosis dan/atau pengobatan penghentian.
• Ketahuilah bahwa jika pasangannya hamil saat pasien menggunakan Revlimid atau segera setelah menghentikan pengobatan Revlimid, mereka harus segera memberi tahu dokter dan merujuk pasangannya ke spesialis atau teratologis yang dapat mengevaluasi situasi dan memberikan pendapat.
Dalam kasus wanita yang berpotensi melahirkan anak, dokter harus memastikan bahwa:
• Pasien memenuhi persyaratan Program Pencegahan Kehamilan, termasuk konfirmasi bahwa dia memiliki tingkat pemahaman yang memadai
• Pasien telah menerima kondisi yang disebutkan di atas
Kontrasepsi
Wanita yang berpotensi melahirkan anak harus menggunakan kontrasepsi yang efektif selama 4 minggu sebelum terapi, selama terapi dan hingga 4 minggu setelah terapi lenalidomide, dan juga dalam hal penghentian dosis, kecuali pasien menyanggupi untuk mengamati "abstinensia absolut dan terus menerus, bulan yang dikonfirmasi. per bulan Jika terapi kontrasepsi yang efektif belum dimulai, pasien harus dirujuk ke dokter spesialis untuk menetapkan metode kontrasepsi yang efektif.
Di bawah ini adalah contoh metode kontrasepsi yang dianggap memadai:
• Tanaman
• Sistem intrauterin pelepas Levonorgestrel (IUS)
• Depot medroksiprogesteron asetat
• Sterilisasi tuba
• Hubungan seksual hanya dengan pasangan pria yang divasektomi; vasektomi harus dikonfirmasi dengan dua analisis air mani negatif
• Pil progestin saja untuk menghambat ovulasi (misalnya desogestrel)
Karena peningkatan risiko tromboemboli vena pada pasien dengan multiple myeloma yang menggunakan lenalidomide dalam rejimen kombinasi, dan pada tingkat yang lebih rendah pada pasien dengan sindrom myelodysplastic dan limfoma sel mantel yang menggunakan lenalidomide saja, penggunaan kontrasepsi oral tidak dianjurkan. juga bagian 4.5). Jika pasien sedang menggunakan kontrasepsi oral kombinasi, ia harus mengganti metode pengendalian kelahiran dengan salah satu metode di atas. Risiko tromboemboli vena tetap selama 4-6 minggu setelah penghentian kontrasepsi oral kombinasi. Kemanjuran steroid kontrasepsi dapat berkurang selama pengobatan bersamaan dengan deksametason (lihat bagian 4.5).
Implan dan sistem intrauterin pelepas Levonorgestrel dikaitkan dengan peningkatan risiko infeksi saat pemasangan, serta perdarahan vagina yang tidak teratur. Profilaksis antibiotik harus dipertimbangkan, terutama pada pasien dengan neutropenia.
Alat kontrasepsi dalam rahim yang melepaskan tembaga umumnya tidak direkomendasikan karena potensi risiko infeksi sejak saat pemasangan dan karena kehilangan darah menstruasi, yang dapat berdampak buruk pada pasien dengan neutropenia atau trombositopenia.
Tes kehamilan
Sesuai dengan praktik setempat, pada pasien dengan potensi subur, tes kehamilan dengan sensitivitas minimum 25 mIU / ml harus dilakukan di bawah pengawasan medis, seperti yang dijelaskan di bawah ini. Kewajiban ini juga berlaku bagi pasien usia subur yang melakukan pantangan secara mutlak dan terus menerus. Idealnya, tes kehamilan, resep dan pengeluaran obat harus dilakukan pada hari yang sama. Lenalidomide harus diberikan kepada pasien yang berpotensi melahirkan anak dalam waktu 7 hari dari tanggal resep.
Sebelum memulai perawatan
Setelah pasien menggunakan kontrasepsi yang efektif setidaknya selama 4 minggu, tes kehamilan yang diawasi secara medis harus dilakukan selama konsultasi di mana lenalidomide diresepkan, atau dalam 3 hari sebelum kunjungan ke dokter. Tes harus memastikan bahwa pasien tidak hamil sebelum memulai pengobatan dengan lenalidomide.
Tindak lanjut dan akhir pengobatan
Tes kehamilan yang diawasi secara medis harus diulang setiap 4 minggu, termasuk 4 minggu setelah akhir pengobatan, kecuali dalam kasus sterilisasi tuba yang dikonfirmasi. Tes kehamilan ini harus dilakukan pada hari yang sama dengan resep dokter atau dalam 3 hari sebelum kunjungan dokter.
Pasien laki-laki
Selama pengobatan, lenalidomide hadir pada tingkat yang sangat rendah dalam air mani dan tidak terdeteksi dalam air mani subyek sehat 3 hari setelah penghentian obat (lihat bagian 5.2). Sebagai tindakan pencegahan dan dengan mempertimbangkan populasi pasien khusus dengan waktu eliminasi yang lama, seperti pasien dengan gangguan ginjal, semua pasien pria yang menggunakan lenalidomide harus menggunakan kondom selama seluruh durasi pengobatan, saat menghentikan pengobatan. terapi, jika pasangan Anda hamil atau berpotensi melahirkan anak dan tidak menggunakan kontrasepsi yang efektif (bahkan jika pria tersebut telah menjalani vasektomi).
Tindakan pencegahan tambahan untuk digunakan
Pasien harus diinstruksikan untuk tidak pernah memberikan obat ini kepada orang lain dan mengembalikan kapsul yang tidak digunakan kepada apoteker pada akhir pengobatan.
Pasien tidak boleh mendonorkan darah selama terapi lenalidomide dan setidaknya satu minggu setelah menghentikan pengobatan.
Materi pendidikan, resep dan pembatasan pengeluaran
Untuk membantu pasien menghindari paparan lenalidomide pada janin, Pemegang Izin Edar akan memberikan materi pendidikan kepada tenaga medis untuk memperkuat peringatan tentang teratogenisitas lenalidomide yang diharapkan, untuk memberi nasihat tentang kontrasepsi sebelum memulai terapi dan untuk memberikan panduan tentang perlunya tes kehamilan . Dokter harus memberi tahu pasien pria dan wanita tentang risiko teratogenik dan tindakan pencegahan kehamilan yang ketat, sebagaimana ditentukan dalam Program Pencegahan Kehamilan, dan memberikan kepada pasien buklet pendidikan yang sesuai, kartu pasien dan / atau instrumen yang setara, sesuai dengan tindakan yang diterapkan di tingkat nasional Sistem kontrol distribusi nasional telah dilaksanakan bekerja sama dengan masing-masing Otoritas Kompeten Nasional Sistem ini menyediakan penggunaan kartu pasien dan/atau instrumen yang setara, untuk kontrol resep dan pengeluaran, dan pengumpulan data rinci berkaitan dengan indikasi, untuk hati-hati mengontrol penggunaan di luar label obat dalam wilayah nasional Idealnya, tes kehamilan, penerbitan resep dan pengeluaran obat harus dilakukan pada hari yang sama. Lenalidomide harus dibagikan kepada pasien yang berpotensi melahirkan dalam waktu 7 hari sejak tanggal resep dan setelah " hasil negatif dari tes kehamilan yang dilakukan di bawah pengawasan medis.
Peringatan khusus tambahan dan tindakan pencegahan untuk digunakan
Gangguan Kardiovaskular
Infark miokard
Kasus infark miokard telah diamati pada pasien yang menerima lenalidomide, terutama pada mereka dengan faktor risiko yang diketahui, dan dalam 12 bulan pertama ketika diberikan dalam kombinasi dengan deksametason. Pasien dengan faktor risiko yang diketahui, termasuk mereka dengan trombosis sebelumnya, harus dipantau secara ketat dan tindakan harus diambil untuk mencoba meminimalkan semua faktor risiko yang dapat dimodifikasi (misalnya merokok, hipertensi, dan hiperlipidemia).
Peristiwa tromboemboli vena dan arteri
Pada pasien dengan multiple myeloma, kombinasi lenalidomide dan deksametason dikaitkan dengan peningkatan risiko tromboemboli vena (terutama trombosis vena dalam dan emboli paru) dan tromboemboli arteri (terutama infark miokard dan kejadian serebrovaskular). tingkat dengan lenalidomide dalam kombinasi dengan melphalan dan prednison pada multiple myeloma yang baru didiagnosis dan sebagai monoterapi pada sindrom myelodysplastic Lihat bagian 4.5 dan 4.8.
Pada pasien dengan sindrom myelodysplastic dan limfoma sel mantel, pengobatan dengan lenalidomide saja juga telah dikaitkan dengan risiko tromboemboli vena (terutama trombosis vena dalam dan emboli paru), tetapi pada tingkat yang lebih rendah dibandingkan pada pasien dengan multiple myeloma - lihat bagian 4.5 dan 4.8.
Oleh karena itu, pasien dengan faktor risiko yang diketahui untuk tromboemboli - termasuk trombosis sebelumnya - harus dipantau secara ketat. Tindakan harus diambil untuk mencoba meminimalkan semua faktor risiko yang dapat dimodifikasi (misalnya merokok, hipertensi, dan hiperlipidemia). Pada pasien ini, pemberian agen eritropoietik secara bersamaan atau riwayat kejadian tromboemboli sebelumnya juga dapat meningkatkan risiko trombosis. Oleh karena itu dianjurkan, pada pasien dengan multiple myeloma yang menggunakan lenalidomide dan deksametason, bahwa agen eritropoietik atau agen lain yang dapat meningkatkan risiko trombosis, seperti misalnya. terapi penggantian hormon. Jika konsentrasi hemoglobin meningkat melebihi 12 g / dl, penggunaan agen eritropoietik harus dihentikan.
Pasien dan dokter harus menyadari perlunya memperhatikan tanda dan gejala tromboemboli. Pasien harus mencari perhatian medis jika gejala seperti sesak napas, nyeri dada, pembengkakan pada tungkai bawah atau atas terjadi. Untuk tujuan profilaksis, asupan obat antitrombotik harus direkomendasikan, terutama pada pasien dengan faktor risiko trombotik tambahan.Keputusan untuk mengadopsi tindakan antitrombotik profilaksis harus dibuat setelah mempertimbangkan faktor risiko untuk setiap pasien secara hati-hati.
Jika pasien mengalami kejadian tromboemboli, pengobatan harus dihentikan dan terapi antikoagulan standar dimulai. Setelah pasien telah stabil pada antikoagulasi dan semua komplikasi dari kejadian tromboemboli telah diselesaikan, pengobatan lenalidomide dapat dilanjutkan dengan dosis awal setelah penilaian manfaat-risiko.Pasien harus melanjutkan terapi antikoagulan selama pengobatan.pengobatan dengan lenalidomide.
Neutropenia dan trombositopenia
Toksisitas pembatas dosis utama lenalidomide termasuk neutropenia dan trombositopenia. Untuk memantau kemungkinan terjadinya sitopenia, jumlah sel darah lengkap, termasuk jumlah sel darah putih termasuk diferensial, jumlah trombosit, hemoglobin dan hematokrit, pada awal, seminggu sekali, harus dilakukan selama 8 minggu pertama pengobatan. lenalidomide, dan sebulan sekali setelahnya.Pada pasien dengan limfoma sel mantel, jadwal pemantauan harus setiap 2 minggu pada siklus 3 dan 4 dan pada awal setiap siklus sesudahnya. Pengurangan dosis mungkin diperlukan (lihat bagian 4.2). Dalam kasus neutropenia, dokter harus mempertimbangkan untuk menggunakan faktor pertumbuhan dalam manajemen pasien. Pasien harus disarankan untuk segera melaporkan episode demam. Perhatian disarankan dalam pemberian lenalidomide secara bersamaan dengan agen mielosupresif lainnya.
• Mieloma multipel yang baru didiagnosis pada pasien yang diobati dengan lenalidomide dalam kombinasi dengan deksametason dosis rendah
Neutropenia tingkat 4 diamati pada tingkat yang lebih rendah pada lenalidomide dalam kombinasi dengan kelompok pengobatan deksametason dosis rendah dibandingkan dengan kelompok pembanding (8,5% di Rd [pengobatan berkelanjutan] dan Rd18 [pengobatan selama 18 siklus empat minggu], dibandingkan dengan 15 siklus. % di lengan melphalan / prednison / thalidomide, lihat bagian 4.8). Episode neutropenia demam derajat 4 konsisten dengan kelompok pembanding (0,6% pada pasien yang diobati dengan lenalidomide/dexamethasone Rd dan Rd18, dibandingkan dengan 0,7% pada pasien pada kelompok melphalan/prednison/thalidomide, lihat bagian 4.8). Pasien harus disarankan untuk segera melaporkan episode demam dan pengurangan dosis mungkin diperlukan (lihat bagian 4.2).
Trombositopenia derajat 3 atau 4 diamati pada tingkat yang lebih rendah pada kelompok Rd dan Rd18 dibandingkan pada kelompok pembanding (masing-masing 8,1% vs 11,1%). Pasien dan dokter harus mengamati tanda dan gejala perdarahan, termasuk petekie dan epistaksis, terutama pada pasien yang menjalani pengobatan bersamaan yang dapat menyebabkan perdarahan (lihat bagian 4.8, Gangguan perdarahan).
• Mieloma multipel yang baru didiagnosis pada pasien yang diobati dengan lenalidomide dalam kombinasi dengan melphalan dan prednison
Dalam studi klinis pada pasien dengan multiple myeloma yang baru didiagnosis, kombinasi lenalidomide dengan melphalan dan prednison dikaitkan dengan insiden yang lebih tinggi dari neutropenia derajat 4 (34,1% pada pasien di kelompok melphalan, prednison dan lenalidomide diikuti oleh lenalidomide [MPR + R] dan melphalan, prednison dan lenalidomide diikuti dengan plasebo [MPR + p], dibandingkan dengan 7,8% pasien yang diobati dengan MPp + p; lihat bagian 4.8. Episode neutropenia demam derajat 4 diamati tidak sering (1,7% pada pasien yang diobati dengan MPR + R / MPR + p, dibandingkan dengan 0,0% pada pasien yang diobati dengan MPp + p; lihat bagian 4.8).
Pada pasien dengan multiple myeloma, kombinasi lenalidomide dengan melphalan dan prednison dikaitkan dengan insiden yang lebih tinggi dari grade 3 dan grade 4 trombositopenia (40,4% pada pasien yang diobati dengan MMR + R / MMR + p, dibandingkan dengan 13,7% pada pasien yang diobati dengan MMR + R / MMR + p, dibandingkan dengan 13,7% pada pasien yang diobati dengan MPp + p; lihat bagian 4.8) Pasien dan dokter harus waspada terhadap tanda dan gejala perdarahan, termasuk petekie dan epistaksis, terutama pada pasien yang diobati secara bersamaan dengan produk obat yang meningkatkan kecenderungan perdarahan (lihat bagian 4.8, Gangguan perdarahan).
• Multiple myeloma dengan setidaknya satu terapi sebelumnya
Pada pasien dengan multiple myeloma yang menerima setidaknya satu terapi sebelumnya, kombinasi lenalidomide dan deksametason dikaitkan dengan insiden neutropenia tingkat 4 yang lebih tinggi (5,1% pasien yang diobati dengan lenalidomide / deksametason dibandingkan dengan 0,6% pasien yang diobati dengan plasebo / deksametason; lihat bagian 4.8) Episode demam neutropenia derajat 4 jarang diamati (pada 0,6% pasien yang diobati dengan lenalidomide / deksametason dibandingkan dengan 0,0% pasien yang diobati dengan plasebo / deksametason; lihat bagian 4.8) Pasien harus disarankan untuk segera melaporkan episode demam Pengurangan dosis mungkin diperlukan (lihat bagian 4.2) Dalam kasus neutropenia, dokter harus mempertimbangkan penggunaan faktor pertumbuhan dalam manajemen pasien.
Pada pasien dengan multiple myeloma, kombinasi lenalidomide dan deksametason dikaitkan dengan insiden yang lebih tinggi dari grade 3 dan grade 4 trombositopenia (9,9% dan 1,4%, masing-masing, insiden yang lebih tinggi dari grade 3 trombositopenia).3 dan Grade 4 (9,9%) dan 1,4% pasien yang diobati dengan lenalidomide / deksametason masing-masing dibandingkan dengan 2,3% dan 0,0% pasien yang diobati dengan plasebo / deksametason; lihat bagian 4.8) Pasien dan dokter harus memantau tanda dan gejala perdarahan, termasuk petekie dan epistaksis, terutama pada pasien diobati secara bersamaan dengan produk obat yang dapat menyebabkan perdarahan (lihat bagian 4.8, Gangguan perdarahan).
• Sindrom mielodisplastik
Pada pasien dengan sindrom myelodysplastic, pengobatan lenalidomide dikaitkan dengan insiden yang lebih tinggi dari tingkat 3 dan 4 neutropenia dan trombositopenia dibandingkan pada pasien yang diobati dengan plasebo (lihat bagian 4.8).
• Limfoma sel mantel
Pada pasien dengan limfoma sel mantel, pengobatan lenalidomide dikaitkan dengan insiden yang lebih tinggi dari tingkat 3 dan 4 neutropenia dibandingkan pada pasien di kelompok kontrol (lihat bagian 4.8).
Infeksi dengan atau tanpa neutropenia
Pasien multiple myeloma rentan terhadap infeksi, termasuk pneumonia. Tingkat infeksi yang lebih tinggi diamati selama pengobatan dengan lenalidomide dalam kombinasi dengan deksametason dibandingkan dengan MPT. Infeksi tingkat 3 terjadi dalam konteks neutropenia pada kurang dari sepertiga pasien. Pasien dengan faktor risiko yang diketahui untuk infeksi harus dipantau secara ketat. Semua pasien harus disarankan untuk berkonsultasi dengan dokter mereka segera pada tanda pertama infeksi (misalnya batuk, demam, dll), untuk memungkinkan intervensi segera untuk mengurangi keparahan.
Gagal ginjal
Lenalidomide secara substansial diekskresikan melalui ginjal. Oleh karena itu, pada pasien dengan insufisiensi ginjal, perhatian khusus harus diberikan dalam pemilihan dosis dan pemantauan fungsi ginjal dianjurkan (lihat bagian 4.2).
Gangguan kelenjar tiroid
Kasus hipotiroidisme dan hipertiroidisme telah diamati. Sebelum memulai pengobatan, kontrol yang optimal dari penyakit penyerta yang mempengaruhi fungsi tiroid dianjurkan. Direkomendasikan bahwa fungsi tiroid dipantau pada awal dan selama pengobatan.
Neuropati perifer
Lenalidomide secara struktural terkait dengan thalidomide, yang diketahui menyebabkan neuropati perifer yang parah. Tidak ada peningkatan neuropati perifer yang diamati dengan penggunaan lenalidomide jangka panjang untuk pengobatan multiple myeloma yang baru didiagnosis.
Reaksi Flare Tumor dan Sindrom Lisis Tumor
Karena lenalidomide menunjukkan aktivitas anti-neoplastik, komplikasi sindrom lisis tumor (Sindrom Lisis Tumor, TL). TLS dan Reaksi Flare Tumor (TFR) umumnya diamati pada pasien dengan leukemia limfositik kronis (CLL) dan jarang diamati pada pasien dengan limfoma yang diobati dengan lenalidomide. Kasus TLS dengan hasil yang fatal telah dilaporkan selama pengobatan dengan lenalidomide. Pasien yang berisiko TLS dan TFR adalah mereka yang memiliki beban tumor tinggi sebelum pengobatan. Perhatian harus dilakukan ketika memulai pengobatan lenalidomide pada pasien ini. Direkomendasikan bahwa pasien tersebut dipantau secara hati-hati, terutama selama siklus pertama atau peningkatan dosis, dan bahwa tindakan pencegahan yang tepat harus diambil.Terdapat laporan yang jarang dari TLS pada pasien dengan MM yang diobati dengan lenalidomide, sementara tidak ada kasus yang dilaporkan pada pasien dengan MDS diobati dengan lenalidomide.
Massa tumor
• Limfoma sel mantel
Lenalidomide tidak dianjurkan untuk pengobatan pasien dengan beban tumor tinggi jika pilihan pengobatan alternatif tersedia.
Kematian dini
Dalam Studi MCL-002 ada peningkatan nyata secara keseluruhan pada kematian dini (dalam 20 minggu). Pasien dengan beban tumor awal yang tinggi memiliki risiko kematian dini yang lebih tinggi: terdapat 16/81 (20%) kematian dini pada kelompok lenalidomide dan 2/28 (7%) kematian dini pada kelompok kontrol. Pada minggu ke-52, angka yang sesuai adalah 32/81 (40%) dan 28/6 (21%) (lihat bagian 5.1).
Kejadian buruk
Dalam Studi MCL-002 selama pengobatan siklus 1, 11/81 (14%) pasien dengan beban tumor tinggi ditarik dari terapi lenalidomide, dibandingkan dengan 1/28 (4%) pada kelompok kontrol. Alasan utama untuk menghentikan pengobatan untuk pasien dengan beban tumor yang tinggi selama pengobatan siklus 1 di kelompok lenalidomide adalah karena efek samping, 7/11 (64%).
Oleh karena itu, pasien dengan beban tumor yang tinggi harus dipantau secara hati-hati untuk reaksi yang merugikan (lihat bagian 4.8), termasuk tanda-tanda Reaksi Flare Tumor (TFR). Untuk penyesuaian dosis dalam kasus TFR, lihat bagian 4.2.
Massa tumor yang meningkat didefinisikan sebagai setidaknya satu lesi dengan diameter 5 cm atau 3 lesi 3 cm.
Reaksi Flare Tumor
• Limfoma sel mantel
Pemantauan dan evaluasi yang cermat untuk TFR direkomendasikan. Pasien dengan peningkatan MIPI (Indeks Prognostik Internasional Limfoma Sel Mantel) pada saat diagnosis atau penyakit yang ditandai dengan massa tumor yang besar (setidaknya satu lesi dengan diameter terpanjang 7 cm) pada awal mungkin berisiko mengalami TFR. Di sana Reaksi Flare Tumor dapat mensimulasikan perkembangan penyakit (PD). Pasien dalam penelitian MCL-002 dan MCL-001 yang mengalami TFR derajat 1 dan 2 diobati dengan kortikosteroid, obat antiinflamasi nonsteroid (NSAID), dan/atau analgesik narkotik untuk pengelolaan gejala TFR. Keputusan untuk mengadopsi tindakan terapeutik untuk TFR harus dibuat setelah "evaluasi klinis yang cermat dari masing-masing pasien (lihat bagian 4.2).
Reaksi alergi
Kasus reaksi alergi / hipersensitivitas telah dilaporkan pada pasien yang diobati dengan lenalidomide (lihat bagian 4.8). Disarankan untuk secara hati-hati memantau pasien yang memiliki reaksi alergi sebelumnya terhadap thalidomide karena kemungkinan reaksi silang antara lenalidomide dan thalidomide telah dilaporkan dalam literatur.
Reaksi kulit yang parah
Kasus SSJ dan NET telah dilaporkan. Pengobatan dengan lenalidomide harus dihentikan jika terjadi ruam eksfoliatif atau bulosa, atau jika dicurigai SSJ atau NET, dan tidak boleh dilanjutkan setelah penghentian karena reaksi ini. Interupsi atau penghentian lenalidomide harus dipertimbangkan untuk bentuk lain dari reaksi kulit tergantung pada tingkat keparahannya.Pasien dengan riwayat ruam parah sebelumnya yang terkait dengan pengobatan thalidomide tidak boleh menerima lenalidomide.
Intoleransi laktosa
Kapsul Revlimid mengandung laktosa. Pasien dengan masalah herediter yang jarang dari intoleransi galaktosa, defisiensi Lapp laktase, atau malabsorpsi glukosa-galaktosa tidak boleh minum obat ini.
Kapsul yang tidak terpakai
Pasien harus disarankan untuk tidak pernah memberikan obat ini kepada orang lain dan mengembalikan kapsul yang tidak digunakan kepada apoteker di akhir pengobatan.
Tumor primer kedua
Peningkatan tumor primer kedua (Sekolah Dasar Kedua Keganasan, SPM) pada pasien myeloma yang sebelumnya diobati dengan lenalidomide / deksametason (3,98 per 100 orang-tahun) dibandingkan kontrol (1,38 per 100 orang-tahun). SPM non-invasif terdiri dari sel basal atau karsinoma sel skuamosa.
Kebanyakan SPM invasif adalah tumor padat.
Dalam studi klinis pada pasien multiple myeloma yang baru didiagnosis yang tidak memenuhi syarat untuk transplantasi, peningkatan 4,9 kali lipat dalam tingkat kejadian PMS hematologis (kasus AML, MDS) diamati pada pasien yang diobati dengan lenalidomide dalam kombinasi dengan melphalan dan prednison untuk perkembangan (1,75 per 100 orang-tahun), dibandingkan dengan melphalan dalam kombinasi dengan prednison (0,36 per 100 per orang-tahun).
Peningkatan 2,12 kali lipat dalam tingkat kejadian SPM padat diamati pada pasien yang diobati dengan lenalidomide (9 siklus) dalam kombinasi dengan melphalan dan prednison (1,57 per 100 orang-tahun), dibandingkan dengan melphalan dalam kombinasi dengan prednison (0,74 per 100 per tahun). orang-tahun).
Pada pasien yang diobati dengan lenalidomide dalam kombinasi dengan deksametason sampai perkembangan atau selama 18 bulan, tingkat kejadian PMS hematologi (0,16 per 100 orang-tahun) tidak meningkat dibandingkan dengan thalidomide dalam kombinasi dengan melphalan dan prednison (0,79 per 100 orang-tahun) .
Peningkatan 1,3 kali lipat dalam tingkat kejadian PMS padat diamati pada pasien yang diobati dengan lenalidomide dalam kombinasi dengan deksametason sampai perkembangan atau selama 18 bulan (1,58 per 100 orang-tahun) dibandingkan dengan thalidomide dalam kombinasi dengan melphalan dan prednison (1,19 per 100 orang-tahun).
Dalam uji klinis pada pasien multiple myeloma yang baru didiagnosis yang memenuhi syarat untuk transplantasi, peningkatan angka kejadian PMS hematologis telah diamati pada pasien yang diobati dengan lenalidomide segera setelah melphalan dosis tinggi dan transplantasi sel induk autologus (Transplantasi Sel Induk Autologus, ASCT), dibandingkan dengan pasien yang diobati dengan plasebo (1,27 hingga 1,56 dan 0,46 hingga 0,53 per 100 orang-tahun, masing-masing). Kasus tumor sel B ganas (termasuk limfoma Hodgkin) diamati dalam uji klinis pada pasien yang diobati dengan lenalidomide dalam pengaturan pasca-ASCT.
Risiko PMS hematologis harus dipertimbangkan sebelum memulai pengobatan dengan Revlimid dalam kombinasi dengan melphalan atau dalam periode segera setelah melphalan dosis tinggi dan ASCT. Dokter harus hati-hati mengevaluasi pasien sebelum dan selama pengobatan, menggunakan skrining kanker standar untuk PMS, dan memulai pengobatan sesuai petunjuk.
Perkembangan menjadi leukemia myeloid akut (AML) pada sindrom myelodysplastic (MDS) berisiko rendah atau menengah-1
• Kariotipe
Variabel dasar termasuk kelainan sitogenetik kompleks dikaitkan dengan perkembangan menjadi AML pada subjek yang bergantung pada transfusi dengan kelainan penghapusan 5q yang terisolasi. Dalam analisis gabungan dari dua studi klinis yang dilakukan dengan Revlimid pada MDS risiko rendah atau menengah-1, subjek dengan kelainan sitogenetik kompleks memiliki risiko kumulatif tertinggi untuk berkembang menjadi AML yang diperkirakan pada 2 tahun (38,6%).Perkiraan laju perkembangan 2 tahun untuk AML pada pasien dengan kelainan penghapusan 5q terisolasi adalah 13,8%, dibandingkan dengan 17,3% untuk pasien dengan kelainan penghapusan 5q terisolasi dan satu "kelainan sitogenetik tambahan.
Akibatnya, rasio manfaat / risiko Revlimid tidak diketahui ketika MDS dikaitkan dengan kelainan penghapusan 5q terisolasi dan kelainan sitogenetik kompleks.
• status TP53
Mutasi TP53 hadir pada 20-25% pasien MDS dengan anomali penghapusan terisolasi 5q risiko rendah dan dikaitkan dengan risiko progresi ke AML yang lebih tinggi. Dalam "analisis post-hoc dari studi klinis (MDS-004) yang dilakukan dengan Revlimid pada MDS risiko rendah atau menengah-1, perkiraan tingkat perkembangan 2 tahun menjadi AML adalah 27,5% pada pasien dengan IHC-p53 positif (1 % cut-off pewarnaan nuklir kuat, menggunakan evaluasi imunohistokimia protein p53 sebagai pengganti status mutasi TP53) dan 3,6% pada pasien dengan IHC-p53 negatif (p = 0,0038) (lihat bagian 4.8).
Progresi ke keganasan lain pada limfoma sel mantel
Pada limfoma sel mantel, AML, tumor sel B ganas dan kanker kulit non-melanoma (NMSC) adalah risiko potensial.
Gangguan hati
Kasus gagal hati, termasuk dengan hasil yang fatal, telah diamati pada pasien yang diobati dengan lenalidomide dalam terapi kombinasi: gagal hati akut, hepatitis toksik, hepatitis sitolitik, hepatitis kolestatik dan hepatitis sitolitik / kolestatik campuran. Mekanisme hepatotoksisitas akibat obat yang parah masih belum diketahui meskipun, dalam beberapa kasus, faktor risiko mungkin penyakit hati virus yang sudah ada sebelumnya, peningkatan enzim hati awal dan kemungkinan pengobatan dengan antibiotik.
Kelainan pada tes fungsi hati umumnya diamati dan umumnya asimtomatik dan reversibel pada penghentian pengobatan. Setelah parameter telah kembali ke nilai dasar, dimulainya kembali pengobatan dengan dosis yang lebih rendah dapat dipertimbangkan.
Lenalidomide diekskresikan melalui ginjal. Penting untuk menyesuaikan dosis pada pasien dengan insufisiensi ginjal untuk menghindari mencapai kadar plasma yang dapat meningkatkan risiko reaksi merugikan hematologis atau hepatotoksisitas yang lebih penting. Pemantauan fungsi hati dianjurkan, terutama dalam kasus infeksi hati virus sebelumnya atau bersamaan atau ketika lenalidomide diberikan dalam kombinasi dengan produk obat yang diketahui terkait dengan disfungsi hati.
Pasien dengan multiple myeloma yang baru didiagnosis
Ada tingkat yang lebih tinggi dari intoleransi (efek samping grade 3 atau 4, efek samping yang serius, penghentian pengobatan) pada pasien berusia> 75 tahun, stadium ISS (Sistem Pementasan Internasional) III, status kinerja (PS) 2 dinilai menurut kriteria ECOG (Grup Onkologi Koperasi Timur) atau CLcr
Katarak
Katarak telah diamati lebih sering pada pasien yang diobati dengan lenalidomide dalam kombinasi dengan deksametason, terutama bila digunakan untuk waktu yang lama. Disarankan untuk secara berkala memantau kemampuan visual.
04.5 Interaksi dengan produk obat lain dan bentuk interaksi lainnya -
Agen eritropoietik, atau agen lain yang dapat meningkatkan risiko trombosis, seperti terapi penggantian hormon, harus digunakan dengan hati-hati pada pasien dengan multiple myeloma yang menggunakan lenalidomide dan deksametason (lihat bagian 4.4 dan 4.8). mengambil lenalidomide dan deksametason (lihat bagian 4.4 dan 4.8).
Kontrasepsi oral
Tidak ada studi interaksi telah dilakukan dengan kontrasepsi oral. Lenalidomide bukanlah penginduksi enzim. Di studio in vitro dilakukan dengan hepatosit manusia, lenalidomide, diuji pada berbagai konsentrasi, tidak menginduksi CYP1A2, CYP2B6, CYP2C9, CYP2C19, dan CYP3A4 / 5. Oleh karena itu, jika lenalidomide diberikan sendiri, induksi yang mengarah pada penurunan kemanjuran produk obat, termasuk kontrasepsi hormonal, tidak diharapkan. Namun, deksametason diketahui sebagai penginduksi CYP3A4 yang lemah hingga sedang dan cenderung mempengaruhi enzim dan protein transpor lainnya. Tidak dikecualikan bahwa kemanjuran kontrasepsi oral dapat dikurangi selama pengobatan.
Langkah-langkah efektif harus diambil untuk menghindari kehamilan (lihat bagian 4.4 dan 4.6).
Warfarin
Pemberian bersama 10 mg dosis berulang lenalidomide tidak berpengaruh pada farmakokinetik dosis tunggal R- dan S-warfarin. Pemberian bersama warfarin 25 mg dosis tunggal tidak berpengaruh pada farmakokinetik lenalidomide. Namun, tidak diketahui apakah ada "interaksi selama" penggunaan klinis (pengobatan bersamaan dengan deksametason). Deksametason adalah penginduksi enzim yang lemah hingga sedang dan efeknya pada warfarin tidak diketahui. Pemantauan ketat konsentrasi warfarin disarankan selama pengobatan.
Digoksin
Pemberian bersama lenalidomide 10 mg / hari meningkatkan konsentrasi plasma digoxin sebesar 14% (0,5 mg, dosis tunggal) dengan CI (interval kepercayaan) 90% [0,52% -28,2% ]. Tidak diketahui apakah efeknya akan berbeda dalam situasi terapeutik (dosis lenalidomide yang lebih tinggi dan pengobatan bersamaan dengan deksametason) Oleh karena itu, pemantauan konsentrasi digoksin dianjurkan selama pengobatan dengan lenalidomide.
Statin
Ketika statin diberikan dengan lenalidomide, ada peningkatan risiko rhabdomyolysis, yang mungkin hanya aditif. Peningkatan pemantauan klinis dan laboratorium diperlukan, terutama selama minggu-minggu pertama pengobatan.
Deksametason
Pemberian bersama dosis tunggal atau ganda deksametason (40 mg / hari) tidak memiliki efek yang relevan secara klinis pada farmakokinetik dosis ganda lenalidomide (25 mg / hari).
Interaksi dengan inhibitor P-glikoprotein (P-gp)
Secara invitro, Lenalidomide adalah substrat P-gp, tetapi bukan inhibitor P-gp. Pemberian bersama beberapa dosis inhibitor P-gp poten, quinidine (600 mg, dua kali sehari) atau inhibitor P-gp kerja sedang / substrat temsirolimus (25 mg), tidak memiliki efek yang relevan secara klinis pada Farmakokinetik lenalidomide (25 mg) Pemberian lenalidomide secara bersamaan tidak mengubah farmakokinetik temsirolimus.
04.6 Kehamilan dan menyusui -
Wanita usia subur / Kontrasepsi pada pria dan wanita
Wanita yang berpotensi melahirkan anak harus menggunakan kontrasepsi yang efektif. Jika kehamilan terjadi selama pengobatan dengan lenalidomide, terapi harus dihentikan dan pasien harus pergi ke spesialis atau berpengalaman dalam teratologi yang dapat menilai situasi dan memberikan pendapat. Jika pasangan pasien laki-laki yang memakai lenalidomide sedang hamil, pasangan harus disarankan untuk pergi ke dokter spesialis atau dokter dengan pengalaman teratologi yang dapat menilai situasi dan memberikan pendapat.
Selama pengobatan, lenalidomide hadir pada tingkat yang sangat rendah dalam air mani dan tidak terdeteksi dalam air mani subyek sehat 3 hari setelah penghentian obat (lihat bagian 5.2). Sebagai tindakan pencegahan dan dengan mempertimbangkan populasi pasien khusus dengan waktu eliminasi yang berkepanjangan, seperti pasien dengan gangguan ginjal, semua pasien laki-laki yang memakai lenalidomide harus menggunakan kondom untuk seluruh durasi pengobatan, selama penangguhan dosis dan hingga satu minggu setelah menghentikan terapi jika pasangan Anda sedang hamil atau berpotensi melahirkan anak dan tidak menggunakan metode kontrasepsi apa pun.
Kehamilan
Lenalidomide secara struktural terkait dengan thalidomide, zat aktif dengan efek teratogenik yang diketahui pada manusia, yang menyebabkan cacat lahir parah yang mengancam jiwa.
Malformasi yang diinduksi Lenalidomide pada monyet mirip dengan yang dijelaskan untuk thalidomide (lihat bagian 5.3). Oleh karena itu, efek teratogenik lenalidomide diharapkan, dan lenalidomide dikontraindikasikan selama kehamilan (lihat bagian 4.3).
Waktunya memberi makan
Karena tidak diketahui apakah lenalidomide diekskresikan dalam ASI, dianjurkan agar menyusui dihentikan selama terapi lenalidomide.
Kesuburan
Sebuah studi kesuburan yang dilakukan pada tikus dengan dosis lenalidomide hingga 500 mg / kg (sekitar 200 hingga 500 kali dosis masing-masing 25 mg dan 10 mg, digunakan pada manusia dan dihitung berdasarkan luas permukaan tubuh) , tidak menunjukkan efek samping pada kesuburan atau toksisitas ibu.
04.7 Efek pada kemampuan mengemudi dan menggunakan mesin -
Lenalidomide memiliki efek ringan atau sedang pada kemampuan mengemudi dan menggunakan mesin. Kelelahan, pusing, mengantuk, pusing dan penglihatan kabur telah dilaporkan selama pengobatan dengan lenalidomide. Oleh karena itu, disarankan untuk berhati-hati saat mengemudikan kendaraan atau menggunakan mesin.
04.8 Efek yang tidak diinginkan -
Ringkasan profil keamanan
Mieloma multipel yang baru didiagnosis pada pasien yang diobati dengan lenalidomide dalam kombinasi dengan deksametason dosis rendah
Efek samping serius yang paling sering diamati (≥ 5%) dengan lenalidomide dalam kombinasi dengan deksametason dosis rendah (Rd dan Rd18), dibandingkan dengan melphalan, prednison dan thalidomide (MPT), adalah:
• Pneumonia (9,8%)
• Gagal ginjal (termasuk akut) (6,3%)
Reaksi merugikan yang diamati lebih sering dengan Rd atau Rd18 dibandingkan dengan MPT adalah: diare (45,5%), kelelahan (32,8%), nyeri punggung (32,0%), asthenia (28,2%), insomnia (27,6%), ruam (24,3%) , nafsu makan menurun (23,1%), batuk (22,7%), demam (21,4%) dan kejang otot (20,5%).
Pasien multiple myeloma yang baru didiagnosis yang diobati dengan lenalidomide dalam kombinasi dengan melphalan dan prednison
Efek samping serius yang paling sering diamati (≥ 5%) dengan melphalan, prednison dan lenalidomide diikuti dengan terapi pemeliharaan dengan lenalidomide (MPR + R) atau melphalan, prednison dan lenalidomide diikuti dengan plasebo (MPR + p), dibandingkan dengan melphalan, prednison dan plasebo diikuti oleh plasebo (MPp + p), adalah:
• Neutropenia demam (6,0%)
• Anemia (5,3%)
Efek samping yang lebih sering diamati dengan MPR + R atau MPR + p dibandingkan dengan MPp + p adalah: neutropenia (83,3%), anemia (70,7%), trombositopenia (70,0%), leukopenia (38, 8%), konstipasi (34,0 %), diare (33,3%), ruam (28,9%), demam (27,0%), edema perifer (25,0%), batuk (24,0%), nafsu makan menurun (23,7%) dan astenia (22,0%).
Multiple myeloma dengan setidaknya satu terapi sebelumnya
Dalam dua studi terkontrol plasebo Fase III, 353 pasien dengan multiple myeloma terpapar pengobatan kombinasi lenalidomide / deksametason dan 351 pasien dengan pengobatan kombinasi plasebo / deksametason.
Reaksi merugikan yang paling serius diamati lebih sering dengan kombinasi lenalidomide / deksametason dibandingkan dengan kombinasi plasebo / deksametason adalah:
• Tromboemboli vena (trombosis vena dalam, emboli paru) (lihat bagian 4.4)
• Neutropenia derajat 4 (lihat bagian 4.4).
Efek samping yang lebih sering terjadi dengan lenalidomide dan deksametason, dibandingkan dengan plasebo dan deksametason, ketika menggabungkan uji klinis multiple myeloma (MM-009 dan MM-010), adalah kelelahan (43,9%), neutropenia, (42,2%), sembelit ( 40,5%), diare (38,5%), kram otot (33,4%), anemia (31,4%), trombositopenia (21,5%) dan ruam (21,2%).
Sindrom mielodisplastik
Profil keamanan keseluruhan Revlimid pada pasien dengan sindrom myelodysplastic didasarkan pada data dari total 286 pasien yang termasuk dalam studi Fase II dan Fase III (lihat bagian 5.1). Pada Fase II, semua 148 pasien menjalani pengobatan lenalidomide. Dalam studi Tahap III, 69 pasien diobati dengan lenalidomide 5 mg, 69 pasien diobati dengan lenalidomide 10 mg, dan 67 pasien menerima plasebo selama fase penelitian double-blind.
Kebanyakan reaksi merugikan cenderung terjadi selama 16 minggu pertama terapi lenalidomide.
Reaksi merugikan yang serius meliputi:
• Tromboemboli vena (trombosis vena dalam, emboli paru) (lihat bagian 4.4)
• Neutropenia derajat 3 atau 4, neutropenia demam, dan trombositopenia derajat 3 atau 4 (lihat bagian 4.4).
Reaksi merugikan yang paling sering diamati yang terjadi lebih sering pada kelompok lenalidomide daripada kelompok kontrol (plasebo) dalam studi Fase III adalah neutropenia, (76,8%), trombositopenia (46,4%), diare (34,8%), sembelit ( 19,6%), mual (19,6%), gatal-gatal (25,4%), ruam (18,1%), kelelahan (18,1%) dan kejang otot (16,7%).
Limfoma sel mantel
Profil keamanan keseluruhan Revlimid pada pasien dengan limfoma sel mantel didasarkan pada data dari 254 pasien yang termasuk dalam studi Fase II acak terkontrol, MCL-002 (lihat bagian 5.1).
Selain itu, reaksi obat yang merugikan (ADR) yang diamati dalam studi pendukung MCL-001 dimasukkan dalam Tabel 3.
Reaksi merugikan serius yang paling sering diamati dalam Studi MCL-002 (dengan perbedaan minimal 2 poin persentase) pada kelompok lenalidomide versus kelompok kontrol adalah:
• Neutropenia (3,6%)
• Emboli paru (3,6%)
• Diare (3,6%)
Reaksi merugikan yang paling sering diamati terjadi lebih sering pada kelompok lenalidomide daripada kelompok kontrol dalam Studi MCL-002 adalah neutropenia, (50,9%), anemia (28,7%), diare (22, 8%), kelelahan (21,0%) , konstipasi (17,4%), pireksia (16,8%) dan ruam (termasuk dermatitis alergi) (16,2%).
Dalam Studi MCL-002 ada peningkatan nyata secara keseluruhan pada kematian dini (dalam 20 minggu). Pasien dengan beban tumor awal yang tinggi memiliki risiko kematian dini yang lebih tinggi: 16/81 (20%) kematian dini pada kelompok lenalidomide dan 2/28 (7%) kematian dini pada kelompok kontrol. Pada minggu ke-52, angka yang sesuai adalah 32/81 (39,5%) dan 28/6 (21%) (lihat bagian 5.1).
Selama pengobatan siklus 1, 11/81 (14%) pasien dengan beban tumor tinggi ditarik dari terapi lenalidomide, dibandingkan dengan 1/28 (4%) pada kelompok kontrol. Alasan utama untuk menghentikan pengobatan untuk pasien dengan beban tumor yang tinggi selama pengobatan siklus 1 di kelompok lenalidomide adalah karena efek samping, 7/11 (64%).
Massa tumor yang meningkat didefinisikan sebagai setidaknya satu lesi dengan diameter 5 cm atau 3 lesi 3 cm.
Daftar ringkasan reaksi yang merugikan
Tabel ringkasan untuk terapi kombinasi
Reaksi merugikan yang diamati pada pasien yang dirawat karena multiple myeloma tercantum di bawah ini berdasarkan kelas dan frekuensi organ sistem. Dalam setiap kelas frekuensi, reaksi merugikan terdaftar dalam urutan penurunan keparahan.Frekuensi didefinisikan sebagai berikut: sangat umum (≥ 1/10); umum (≥ 1/100,
Tabel berikut disusun berdasarkan data yang dikumpulkan selama studi multiple myeloma dengan terapi kombinasi. Data belum diperbarui dengan mempertimbangkan durasi pengobatan yang lebih lama pada kelompok yang mengandung lenalidomide berlanjut sampai perkembangan penyakit, dibandingkan dengan kelompok pembanding dalam studi multiple myeloma yang penting (lihat bagian 5.1).
Reaksi yang merugikan ditempatkan dalam kategori yang sesuai dalam tabel di bawah ini, menurut insiden tertinggi yang diamati di salah satu studi klinis penting.
Tabel 1: Reaksi merugikan yang dilaporkan dalam uji klinis pada pasien multiple myeloma yang diobati dengan lenalidomide dalam kombinasi dengan deksametason, atau dengan melphalan dan prednison
^ Lihat bagian 4.8 Deskripsi reaksi merugikan yang dipilih
* Kanker kulit sel skuamosa diamati dalam uji klinis pada pasien myeloma yang sebelumnya diobati dengan lenalidomide / deksametason dibandingkan dengan kontrol
** Kanker kulit sel skuamosa diamati dalam studi klinis pada pasien myeloma yang baru didiagnosis dengan lenalidomide / deksametason dibandingkan dengan kontrol
Tabel ringkasan untuk monoterapi
Reaksi merugikan yang diamati pada pasien yang dirawat karena sindrom myelodysplastic dan limfoma sel mantel tercantum di bawah ini berdasarkan kelas dan frekuensi organ sistem.
Dalam setiap kelas frekuensi, reaksi merugikan diurutkan berdasarkan tingkat keparahannya.Frekuensi didefinisikan sebagai: sangat umum (≥ 1/10); umum (≥ 1/100,
Tabel berikut telah disusun berdasarkan data yang dikumpulkan selama studi monoterapi utama untuk sindrom myelodysplastic dan limfoma sel mantel.
Reaksi yang merugikan ditempatkan dalam kategori yang sesuai dalam tabel berikut, menurut insiden tertinggi yang diamati di salah satu studi klinis penting.
Tabel 2: Efek samping yang dilaporkan dalam uji klinis pada pasien dengan sindrom myelodysplastic yang diobati dengan lenalidomide
^ Lihat bagian 4.8 Deskripsi reaksi merugikan yang dipilih
Efek samping yang diamati sebagai serius dalam uji klinis sindrom myelodysplastic.
Perubahan mood diamati sebagai efek samping serius yang umum dalam studi sindrom myelodysplastic Fase III; tidak dilaporkan sebagai efek samping grade 3 atau 4.
Algoritma yang diterapkan untuk entri SmPC: Semua reaksi obat yang merugikan (ADR) yang ditangkap oleh algoritma studi Fase III termasuk dalam SmPC Eropa. Untuk ADR ini, kontrol tambahan dari frekuensi ADR yang diperoleh oleh algoritma studi Fase II dilakukan dan, jika frekuensi ADR dalam studi Fase II lebih tinggi dari yang tercatat dalam studi Fase III, peristiwa tersebut termasuk dalam CPR Eropa pada frekuensi yang diamati dalam studi Fase II.
Algoritma yang diterapkan untuk sindrom myelodysplastic:
• Studi fase III pada sindrom myelodysplastic (populasi keamanan double-blind, perbedaan antara lenalidomide 5/10 mg dan plasebo untuk rejimen dosis awal dengan kejadian pada setidaknya 2 subjek))
o Semua efek samping yang terjadi selama pengobatan pada 5% dari subyek yang diobati dengan lenalidomide dan perbedaan minimal 2% dalam persentase antara lenalidomide dan plasebo
o Semua efek samping Grade 3 atau 4 yang terjadi selama pengobatan pada 1% subjek yang diobati dengan lenalidomide dan perbedaan setidaknya 1% dalam persentase antara lenalidomide dan plasebo
o Semua efek samping serius yang terjadi selama pengobatan pada 1% subjek yang diobati dengan lenalidomide dan perbedaan setidaknya 1% dalam persentase antara lenalidomide dan plasebo
• Studi fase II tentang sindrom myelodysplastic
o Semua efek samping yang terjadi selama pengobatan pada 5% dari subjek yang diobati dengan lenalidomide o Semua efek samping tingkat 3 atau 4 yang terjadi selama pengobatan pada 1% dari subjek yang diobati dengan lenalidomide o Semua efek samping serius yang terjadi selama pengobatan pada 1% dari subjek yang diobati dengan lenalidomide
Tabel 3: Reaksi merugikan yang dilaporkan dalam uji klinis pada pasien dengan limfoma sel mantel yang diobati dengan lenalidomide
^ Lihat bagian 4.8 Deskripsi reaksi merugikan yang dipilih
Efek samping yang diamati sebagai serius dalam uji klinis limfoma sel mantel.
Algoritma yang diterapkan untuk limfoma sel mantel:
• Studi terkontrol fase II pada limfoma sel mantel
o Semua efek samping yang terjadi selama pengobatan pada 5% subjek dalam kelompok lenalidomide dan perbedaan minimal 2% dalam persentase antara lenalidomide dan kelompok kontrol
o Semua efek samping Grade 3 atau 4 yang terjadi selama pengobatan pada 1% subjek dalam kelompok lenalidomide dan perbedaan setidaknya 1,0% dalam persentase antara lenalidomide dan kelompok kontrol
o Semua efek samping serius yang terjadi selama pengobatan pada 1% subjek dalam kelompok lenalidomide dan perbedaan setidaknya 1,0% dalam persentase antara lenalidomide dan kelompok kontrol
• Studi lengan tunggal fase II pada limfoma sel mantel
o Semua efek samping yang terjadi selama pengobatan pada 5% subjek
o Semua efek samping Grade 3 atau 4 yang terjadi selama pengobatan dilaporkan pada 2 atau lebih subjek
Tabel ringkasan reaksi merugikan pasca pemasaran
Selain reaksi merugikan yang disebutkan di atas yang diidentifikasi dari studi klinis penting, tabel berikut telah disusun berdasarkan data yang dikumpulkan dari pasca-pemasaran.
Tabel 4: Efek samping yang dilaporkan dalam penggunaan pasca-pemasaran pada pasien yang diobati dengan lenalidomide
^ Lihat bagian 4.8 Deskripsi reaksi merugikan yang dipilih
Deskripsi reaksi merugikan yang dipilih
Teratogenisitas
Lenalidomide secara struktural terkait dengan thalidomide, zat aktif dengan efek teratogenik yang diketahui pada manusia, yang menyebabkan cacat lahir parah yang mengancam jiwa. Lenalidomide menyebabkan malformasi pada monyet mirip dengan yang dijelaskan untuk thalidomide (lihat bagian 4.6 dan 5.3). diharapkan pada manusia selama kehamilan.
Neutropenia dan trombositopenia
• Pasien multiple myeloma yang baru didiagnosis diobati dengan lenalidomide dalam kombinasi dengan deksametason dosis rendah
Pada pasien dengan multiple myeloma yang baru didiagnosis, kombinasi lenalidomide dengan deksametason dosis rendah dikaitkan dengan penurunan insiden neutropenia tingkat 4 (8,5% di Rd dan Rd18, dibandingkan dengan 15% di MPT).Neutropenia demam Tingkat 4 jarang diamati (0,6%, dibandingkan dengan 0,7% di MPT).
Pada pasien dengan multiple myeloma yang baru didiagnosis, kombinasi lenalidomide dengan deksametason dosis rendah dikaitkan dengan penurunan insiden trombositopenia grade 3 dan 4 (8,1% pada Rd dan Rd18, dibandingkan dengan 11% pada MPT).
• Pasien multiple myeloma yang baru didiagnosis yang diobati dengan lenalidomide dalam kombinasi dengan melphalan dan prednison
Pada pasien dengan multiple myeloma yang baru didiagnosis, kombinasi lenalidomide dengan melphalan dan prednison dikaitkan dengan insiden yang lebih tinggi dari neutropenia derajat 4 (34,1% pada MMR + R / MPR + p, dibandingkan dengan 7,8% pada MPp + p) Insiden yang lebih tinggi neutropenia derajat 4 demam diamati (1,7% pada MPR + R / MPR + p, dibandingkan dengan 0,0% pada MPp + p).
Pada pasien dengan multiple myeloma yang baru didiagnosis, kombinasi lenalidomide dengan melphalan dan prednison dikaitkan dengan insiden trombositopenia grade 3 dan grade 4 yang lebih tinggi (40,4% pada pasien yang diobati dengan MMR + R / MMR + p , dibandingkan dengan 13,7% pada pasien diobati dengan MPp + p).
• Multiple myeloma dengan setidaknya satu terapi sebelumnya
Pada pasien dengan multiple myeloma, kombinasi lenalidomide dan deksametason dikaitkan dengan insiden neutropenia tingkat 4 yang lebih tinggi (5,1% pasien yang diobati dengan lenalidomide / deksametason versus 0,6% pasien yang diobati dengan plasebo / deksametason. Episode neutropenia demam tingkat 4 jarang diamati ( pada 0,6% pasien yang diobati dengan lenalidomide / deksametason versus 0,0% pasien yang diobati dengan plasebo / deksametason).
Pada pasien dengan multiple myeloma, kombinasi lenalidomide dan deksametason dikaitkan dengan insiden yang lebih tinggi dari tingkat 3 dan tingkat 4 trombositopenia (pada 9,9% dan 1,4% dari pasien yang diobati dengan lenalidomide / deksametason, masing-masing dibandingkan dengan 2,3% dan 0,0% dari pasien yang diobati dengan plasebo / deksametason).
• Sindrom mielodisplastik
Pada pasien dengan sindrom myelodysplastic, lenalidomide dikaitkan dengan insiden neutropenia derajat 3 atau 4 yang lebih tinggi (74,6% pasien yang diobati dengan lenalidomide versus 14,9% pasien yang diobati dengan plasebo dalam studi Fase III). Derajat 3 atau 4 episode neutropenia demam diamati pada 2,2% pasien yang diobati dengan lenalidomide dibandingkan dengan 0,0% pasien yang diobati dengan plasebo. Lenalidomide dikaitkan dengan insiden yang lebih tinggi dari trombositopenia grade 3 atau 4 (37% pada pasien yang diobati dengan lenalidomide versus 1,5% pada pasien yang diobati dengan plasebo dalam studi Fase III).
• Limfoma sel mantel
Pada pasien dengan limfoma sel mantel, lenalidomide dikaitkan dengan insiden neutropenia derajat 3 atau 4 yang lebih tinggi (43,7% pasien yang diobati dengan lenalidomide dibandingkan dengan 33,7% pasien pada kelompok kontrol dalam studi Fase III). Derajat 3 atau 4 episode neutropenia demam diamati pada 6,0% pasien yang diobati dengan lenalidomide dibandingkan dengan 2,4% pasien pada kelompok kontrol.
Tromboemboli vena
Peningkatan risiko deep vein thrombosis (DVT) dan emboli paru (PE) dikaitkan dengan penggunaan lenalidomide dan deksametason pada pasien dengan multiple myeloma dan, pada tingkat lebih rendah, pada pasien yang diobati dengan melphalan dan prednison atau sebagai monoterapi pada pasien dengan sindrom myelodysplastic dan limfoma sel mantel diobati dengan lenalidomide (lihat bagian 4.5) Pada pasien ini, pemberian agen eritropoietik secara bersamaan atau riwayat DVT sebelumnya juga dapat meningkatkan risiko trombosis.
Infark miokard
Kasus infark miokard telah diamati pada pasien yang menerima lenalidomide, terutama pada mereka dengan faktor risiko yang diketahui.
Gangguan perdarahan
Gangguan perdarahan terdaftar di bawah klasifikasi yang berbeda berdasarkan organ yang terlibat: patologi darah dan sistem limfatik; patologi sistem saraf (perdarahan intrakranial); patologi pernapasan, toraks dan mediastinum (epistaksis); patologi gastrointestinal (perdarahan gingiva, perdarahan hemoroid, perdarahan rektal); kelainan ginjal dan saluran kemih (hematuria); trauma, keracunan dan komplikasi prosedural (memar); kelainan pembuluh darah (ecchymosis).
Reaksi alergi
Kasus reaksi alergi / hipersensitivitas telah dilaporkan. Kemungkinan reaksi silang antara lenalidomide dan thalidomide telah dilaporkan dalam literatur.
Reaksi kulit yang parah
Kasus SSJ dan NTE telah dilaporkan. Pasien dengan riwayat ruam parah sebelumnya yang terkait dengan pengobatan thalidomide tidak boleh menerima lenalidomide.
Tumor primer kedua
* Dalam uji klinis pada pasien myeloma yang sebelumnya diobati dengan lenalidomide / dexamethasone versus kontrol, terutama terdiri dari sel basal atau kanker kulit sel skuamosa.
Leukemia mieloid akut
• Mieloma multipel
Dalam uji klinis pada multiple myeloma yang baru didiagnosis, kasus AML telah diamati pada pasien yang diobati dengan lenalidomide dalam kombinasi dengan melphalan, atau segera setelah melphalan dosis tinggi dan ASCT (lihat bagian 4.4). Peningkatan ini tidak diamati dalam uji klinis pada pasien multiple myeloma yang baru didiagnosis yang diobati dengan lenalidomide dalam kombinasi dengan deksametason dosis rendah, dibandingkan dengan thalidomide dalam kombinasi dengan melphalan dan prednison.
• Sindrom mielodisplastik
Variabel dasar termasuk kelainan sitogenetik kompleks dan mutasi TP53 dikaitkan dengan perkembangan menjadi AML pada subjek yang bergantung pada transfusi dengan kelainan delesi 5q yang terisolasi (lihat bagian 4.4). Risiko kumulatif perkembangan menjadi AML yang diperkirakan dalam 2 tahun adalah 13,8% pada pasien dengan kelainan penghapusan 5q terisolasi, dibandingkan dengan 17,3% untuk pasien dengan kelainan penghapusan 5q terisolasi dan satu "kelainan sitogenetik tambahan. , dan 38,6% pada pasien dengan kariotipe kompleks.
Dalam "analisis post-hoc dari studi klinis yang dilakukan dengan Revlimid pada sindrom myelodysplastic, perkiraan tingkat perkembangan 2 tahun menjadi AML adalah 27,5% pada pasien IHC-p53-positif dan 3,6% pada pasien IHC-p53-positif. IHC- p53-negatif (p = 0,0038) Pada pasien IHC-p53-positif, tingkat perkembangan AML yang lebih rendah diamati di antara mereka yang mencapai respons kemandirian transfusi (11,1%) , dibandingkan dengan non-penanggap (34,8%).
Gangguan hati
Reaksi merugikan pasca pemasaran berikut telah diamati (frekuensi tidak diketahui): gagal hati akut dan kolestasis (keduanya mengancam jiwa), hepatitis toksik, hepatitis sitolitik, hepatitis campuran sitolitik / kolestatik.
Rhabdomyolisis
Kasus rhabdomyolysis yang jarang telah diamati, beberapa di antaranya ketika lenalidomide diberikan dengan statin.
Gangguan kelenjar tiroid
Kasus hipotiroidisme dan hipertiroidisme telah diamati (lihat bagian 4.4 Gangguan tiroid).
Reaksi Flare Tumor dan Sindrom Lisis Tumor
Dalam Studi MCL-002, sekitar 10% pasien yang diobati dengan lenalidomide mengalami TFR, dibandingkan dengan 0% pada kelompok kontrol. Sebagian besar kejadian terjadi pada siklus 1, semuanya dinilai terkait pengobatan, dan sebagian besar laporan adalah Grade 1 atau 2. Pasien dengan MIPI tinggi saat diagnosis dan penyakit yang ditandai dengan massa tumor yang besar (setidaknya satu lesi dengan diameter terpanjang 7 cm ) pada awal mungkin berisiko untuk TFR. Dalam studi MCL-002, TLS dilaporkan untuk satu pasien di masing-masing dari dua kelompok pengobatan. Dalam studi dukungan MCL-001, sekitar 10% subjek mengalami TFR; semua laporan adalah Grade 1 atau 2 dalam tingkat keparahan dan semuanya dinilai berhubungan dengan pengobatan. Sebagian besar kejadian terjadi pada siklus 1. Tidak ada laporan TLS pada penelitian MCL-001 (lihat bagian 4.4).
Gangguan gastrointestinal
Perforasi gastrointestinal, yang dapat menyebabkan komplikasi septik dan dapat dikaitkan dengan hasil yang fatal, telah diamati selama pengobatan lenalidomide.
Pelaporan dugaan reaksi merugikan
Pelaporan dugaan reaksi merugikan yang terjadi setelah otorisasi produk obat adalah penting karena memungkinkan pemantauan berkelanjutan dari keseimbangan manfaat / risiko produk obat. Profesional kesehatan diminta untuk melaporkan setiap dugaan reaksi merugikan melalui sistem pelaporan nasional. di "Lampiran V .
04.9 Overdosis -
Tidak ada pengalaman khusus dalam pengelolaan overdosis lenalidomide pada pasien, meskipun dalam studi pengaturan dosis beberapa pasien terkena dosis hingga 150 mg dan, dalam studi dosis tunggal, beberapa pasien terkena dosis hingga 400 mg. Dalam studi ini, toksisitas pembatas dosis pada dasarnya bersifat hematologis. Dalam kasus overdosis, terapi suportif dianjurkan.
05.0 SIFAT FARMAKOLOGI -
05.1 "Sifat farmakodinamik -
Kelompok farmakoterapi: imunosupresan lainnya.
Kode ATC: L04 AX04.
Mekanisme aksi
Mekanisme kerja lenalidomide termasuk sifat anti-neoplastik, anti-angiogenik, pro-eritropoietik dan imunomodulator. Secara khusus, lenalidomide menghambat proliferasi sel tumor hematopoietik spesifik (termasuk sel plasma kanker MM dan sel dengan delesi kromosom 5). , meningkatkan imunitas yang diperantarai sel T dan sel pembunuh alami (NK) dan meningkatkan jumlah sel NKT; menghambat angiogenesis dengan menghalangi migrasi dan adhesi sel endotel dan pembentukan pembuluh mikro; meningkatkan produksi hemoglobin janin oleh sel punca hematopoietik CD34 +, dan menghambat produksi sitokin proinflamasi (misalnya TNF-α dan IL-6) oleh monosit.
Dalam MDS dengan anomali penghapusan 5q terisolasi, lenalidomide telah terbukti secara selektif menghambat klon abnormal, meningkatkan apoptosis sel Del (5q).
Lenalidomide berikatan langsung dengan cereblon, sebuah komponen kompleks enzim cullin-RING E3 ubiquitin ligase, yang meliputi deoxyribonucleic acid (DNA) damage binding protein 1 (DDB1,Protein Pengikat Kerusakan DNA-1), cullin 4 (CUL4) dan culling regulator 1 (Roc1). Dengan adanya lenalidomide, cereblon berikatan dengan protein substrat Aiolos dan Ikaros, yang merupakan faktor transkripsi limfoid, menyebabkan ubiquitinasi dan degradasi selanjutnya, dengan konsekuensi sitotoksik dan efek imunomodulator.
Kemanjuran dan keamanan klinis
Lenalidomide telah dievaluasi dalam dua studi Fase III pada multiple myeloma yang baru didiagnosis dan dalam dua studi Fase III pada multiple myeloma refrakter yang kambuh, seperti yang dijelaskan di bawah ini.
Aku Dan L atau M multipel yang baru didiagnosis
Lenalidomide dalam kombinasi dengan deksametason pada pasien yang tidak memenuhi syarat untuk transplantasi sel induk
Kemanjuran dan keamanan lenalidomide dievaluasi dalam studi Fase III multisenter, acak, label terbuka, tiga lengan (MM-020) pada pasien yang berusia 65 tahun atau lebih atau, jika berusia di bawah 65 tahun, yang tidak memenuhi syarat untuk transplantasi sel induk karena keputusan pasien atau tidak tersedianya transplantasi sel induk karena biaya atau alasan lain. Penelitian (MM-020) membandingkan lenalidomide dan deksametason (Rd) yang diberikan untuk 2 durasi pengobatan yang berbeda (misalnya sampai perkembangan penyakit [lengan Rd] atau hingga delapan belas siklus 28 hari [72 minggu, kelompok Rd18]) dengan melphalan, prednison dan thalidomide (MPT) hingga dua belas siklus 42 hari (72 minggu). Pasien diacak (1: 1: 1) ke salah satu dari 3 kelompok pengobatan. Pada pengacakan, pasien dikelompokkan berdasarkan usia (≤ 75 tahun vs> 75 tahun), stadium (ISS stadium I dan II vs stadium III), dan negara.
Pasien dalam kelompok Rd dan Rd18 menerima lenalidomide 25 mg sekali sehari pada Hari 1 hingga 21 dari siklus 28 hari, menurut kelompok protokol. Deksametason 40 mg diberikan sekali sehari pada Hari 1, 8, 15, dan 22 dari setiap siklus pengobatan 28 hari. Dosis awal dan rejimen untuk Rd dan Rd18 disesuaikan dengan usia dan fungsi ginjal (lihat bagian 4.2) Pasien berusia> 75 tahun menerima dosis deksametason 20 mg sekali sehari pada Hari 1, 8, 15 dan 22 setiap 28 hari siklus pengobatan Semua pasien menjalani profilaksis antikoagulan (heparin berat molekul rendah, warfarin, heparin, aspirin dosis rendah) selama penelitian.
Titik akhir efikasi utama dalam penelitian ini adalah kelangsungan hidup bebas perkembangan (Kemajuan Kelangsungan Hidup Gratis, PF). Secara total, 1623 pasien terdaftar dalam penelitian ini: 535 pasien diacak ke Rd, 541 pasien diacak ke Rd18, dan 547 pasien diacak ke MPT. Karakteristik demografis pasien dan terkait penyakit pada awal seimbang di ketiga kelompok.Secara keseluruhan, subjek penelitian memiliki penyakit lanjut: dari total populasi penelitian, 41% berada di ISS stadium III, 9% memiliki gangguan ginjal berat (klirens kreatinin [CLcr]
Dalam analisis terbaru PFS, PFS2, dan kelangsungan hidup keseluruhan (OS) menggunakan tanggal cut-off 3 Maret 2014, di mana waktu tindak lanjut rata-rata untuk semua subjek yang bertahan adalah 45,5 bulan, hasil penelitian disajikan dalam Tabel 5.
Tabel 5: Ringkasan data efikasi secara keseluruhan
AMT = terapi antimieloma; CI = selang kepercayaan; CR = tanggapan lengkap; d = deksametason dosis rendah; HR = rasio bahaya; IMWG = Kelompok Kerja Mieloma Internasional; IRAC = Komite Ajudikasi Respon Independen; M = melphalan; maks = maksimum; min = minimal; NS = tidak dapat diperkirakan; OS = kelangsungan hidup secara keseluruhan; P = prednison; PFS = kelangsungan hidup bebas perkembangan; PR = tanggapan parsial; R = lenalidomida; Rd = Rd diberikan sampai perkembangan penyakit terdokumentasi; Rd18 = Rd diberikan selama 18 siklus; SE = kesalahan standar; T = talidomid; VGPR = respons parsial optimal; vs = lawan.
a Median didasarkan pada perkiraan Kaplan-Meier.
b 95% CI tentang median.
c Berdasarkan model bahaya proporsional Cox yang membandingkan fungsi bahaya yang terkait dengan kelompok pengobatan yang ditunjukkan.
d Nilai-p didasarkan pada uji log rank unstratified dari perbedaan kurva Kaplan-Meier antara kelompok perlakuan yang ditunjukkan.
e Titik akhir eksplorasi (PFS2)
f Median adalah statistik univariat tanpa koreksi pemotongan.
g Peningkatan penilaian tanggapan yang diputuskan selama fase pengobatan penelitian (untuk definisi setiap kategori tanggapan Tanggal batas data = 24 Mei 2013).
h Tanggal batas = 24 Mei 2013
Lenalidomide dalam kombinasi dengan melphalan dan prednison, diikuti dengan monoterapi pemeliharaan, di pasien yang tidak memenuhi syarat untuk transplantasi
Keamanan dan kemanjuran lenalidomide (MPR) dievaluasi dalam studi Fase III multisenter, acak, double-blind, 3-lengan (MM-015) pada pasien berusia 65 tahun ke atas dan dengan kreatinin serum. 75 tahun) dan stadium (ISS tahap I dan II vs tahap III).
Penelitian ini mengkaji penggunaan terapi kombinasi MMR (melphalan 0,18 mg/kg BB peroral pada hari ke 1-4 dari ulangan 28 hari siklus; prednison 2 mg/kg BB peroral pada hari ke 1-4 dari ulangan 28 hari siklus; dan lenalidomide 10 mg / hari secara oral pada hari ke 1-21 siklus 28 hari berulang), untuk terapi induksi, maksimal 9 siklus, Pasien yang telah menyelesaikan 9 siklus, atau yang tidak dapat menyelesaikan 9 siklus karena intoleransi, beralih ke monoterapi pemeliharaan, dimulai dengan lenalidomide 10 mg secara oral pada hari 1-21 dari siklus 28 hari berulang, sampai perkembangan penyakit
Titik akhir kemanjuran utama dalam penelitian ini adalah kelangsungan hidup bebas perkembangan (PFS).Secara total, 459 pasien terdaftar dalam penelitian: 152 pasien diacak untuk MMR + R, 153 pasien diacak untuk MMR + p dan 154 pasien diacak untuk MPp + p Karakteristik demografi pasien dan terkait penyakit pada awal seimbang di ketiga kelompok; khususnya, sekitar 50% pasien yang terdaftar di setiap kelompok memiliki karakteristik berikut: ISS stadium III dan bersihan kreatinin
Dalam "analisis PFS, PFS2 dan OS menggunakan cut-off date April 2013, median waktu tindak lanjut untuk semua subjek yang bertahan hidup adalah 62,4 bulan, hasil penelitian disajikan pada Tabel 6. .
Tabel 6: Ringkasan data efikasi secara keseluruhan
CI = selang kepercayaan; CR = tanggapan lengkap; HR = rasio bahaya; M = melphalan; NS = tidak dapat diperkirakan; OS = kelangsungan hidup secara keseluruhan; p = plasebo; P = prednison;
PD = penyakit progresif; PR = tanggapan parsial; R = lenalidomida; SD = penyakit stabil; VGPR = respons parsial optimal.
a Median didasarkan pada perkiraan Kaplan-Meier.
PFS2 (titik akhir eksplorasi) didefinisikan untuk semua pasien (ITT) sebagai waktu dari pengacakan hingga inisiasi terapi anti-myeloma lini ketiga atau kematian karena sebab apa pun, untuk semua pasien acak
Studi pendukung pada multiple myeloma yang baru didiagnosis
Sebuah open-label, acak, studi Fase III multicenter (ECOG E4A03) dilakukan pada 445 pasien dengan multiple myeloma yang baru didiagnosis; 222 pasien diacak ke kelompok lenalidomide / deksametason dosis rendah dan 223 diacak ke kelompok lenalidomide / dosis standar deksametason. Pasien yang diacak dalam kelompok lenalidomide / dosis standar deksametason menerima lenalidomide 25 mg / hari pada hari 1 hingga 21, setiap 28 hari, ditambah deksametason 40 mg / hari pada hari 1 hingga 4, 9 hingga 12 dan 17 pada 20, setiap 28 hari, untuk empat siklus pertama. Pasien yang diacak pada kelompok lenalidomide / deksametason dosis rendah menerima lenalidomide 25 mg / hari pada hari 1 hingga 21, setiap 28 hari, ditambah deksametason dosis rendah 40 mg / hari pada hari 1, 8, 15, dan 22, masing-masing 28 hari . Pada kelompok lenalidomide/dexamethasone dosis rendah, 20 pasien (9,1%) mengalami setidaknya satu interupsi dosis dibandingkan dengan 65 pasien (29,3%) pada kelompok lenalidomide/dexamethasone dosis standar.
Dalam analisis post-hoc, mortalitas terendah diamati pada kelompok lenalidomide / deksametason dosis rendah 6,8% (15/220), dibandingkan dengan kelompok lenalidomide / deksametason dosis standar 19,3% (43/223 ), pada kelompok multipel yang baru didiagnosis. populasi pasien myeloma, dengan median tindak lanjut 72,3 minggu.
Namun, dengan tindak lanjut yang diperpanjang, perbedaan kelangsungan hidup secara keseluruhan yang mendukung lenalidomide / deksametason dosis rendah cenderung menurun.
Multiple myeloma dengan setidaknya satu terapi sebelumnya
Kemanjuran dan keamanan lenalidomide dievaluasi dalam dua studi multisenter Fase III, acak, double-blind, terkontrol plasebo, kelompok paralel (MM-009 dan MM-010) dari lenalidomide dalam kombinasi dengan deksametason versus monoterapi Dexamethasone pada pasien yang sebelumnya diobati dengan multiple myeloma. Dari 353 pasien yang termasuk dalam studi MM-009 dan MM-010 yang diobati dengan lenalidomide / deksametason, 45,6% berusia 65 tahun atau lebih. Dari 704 pasien yang dievaluasi dalam studi MM-009 dan MM-010, 44,6% adalah 65 tahun atau lebih.
Dalam kedua penelitian, pasien dalam kelompok lenalidomide / deksametason (len / des) menerima lenalidomide 25 mg secara oral sekali sehari pada hari 1 hingga 21 dan kapsul plasebo yang tampak identik sekali sehari. hari ke 22 hingga 28 dari setiap siklus 28 hari Pasien dalam Kelompok plasebo / deksametason (plasebo / des) mengambil 1 kapsul plasebo pada hari 1 hingga 28 setiap siklus 28 hari. Pasien pada kedua kelompok mengambil 40 mg deksametason secara oral sekali sehari pada hari 1 sampai 4, 9 sampai 12 dan
17 hingga 20 dari setiap siklus 28 hari, untuk 4 siklus pertama terapi. Setelah 4 program terapi pertama, dosis deksametason dikurangi menjadi 40 mg per oral sekali sehari pada hari 1 sampai 4 dari setiap siklus 28 hari.Dalam kedua studi, pengobatan dilanjutkan sampai perkembangan penyakit Penyesuaian dosis diperbolehkan di kedua studi berdasarkan temuan klinis dan laboratorium.
Titik akhir efikasi utama dalam kedua studi adalah waktu untuk perkembangan penyakit (TTP, waktu untuk kemajuan). Sebanyak 353 pasien dievaluasi dalam penelitian MM-009: 177 pada kelompok lenalidomide / deksametason dan 176 pada kelompok plasebo / deksametason. Sebanyak 351 pasien dievaluasi dalam penelitian MM-010: 176 pada kelompok lenalidomide / deksametason dan 175 pada kelompok plasebo / deksametason.
Dalam kedua studi, kelompok lenalidomide / deksametason dan plasebo / deksametason memiliki karakteristik demografis awal dan terkait penyakit yang sebanding. Kedua populasi pasien memiliki usia rata-rata 63 tahun, dengan rasio yang sebanding antara pasien pria dan wanita.Grup Onkologi Koperasi Timur), baik jumlah dan jenis terapi sebelumnya sebanding pada kedua kelompok.
Analisis interim dijadwalkan sebelumnya untuk kedua studi menunjukkan bahwa terapi kombinasi lenalidomide / deksametason menunjukkan peningkatan yang signifikan secara statistik (hal.
Analisis efikasi tindak lanjut yang diperpanjang dilakukan selama rata-rata 130,7 minggu Tabel 7 menunjukkan hasil analisis efikasi tindak lanjut - studi bersama MM-009 dan MM-010.
Dalam analisis lanjutan yang diperluas ini, TTP median adalah 60,1 minggu (95% CI: 44,3, 73,1) pada pasien yang diobati dengan lenalidomide / deksametason (N = 353) dibandingkan dengan median 20 , 1 minggu (95% CI: 17,7, 20,3) pada pasien yang diobati dengan plasebo / deksametason (N = 351). Kelangsungan hidup bebas perkembangan rata-rata adalah 48,1 minggu (95% CI: 36,4, 62,1) pada pasien yang diobati dengan lenalidomide / deksametason dibandingkan dengan waktu rata-rata 20,0 minggu (95% CI: 16, 1, 20,1) pada pasien yang diobati dengan plasebo / deksametason . Durasi pengobatan rata-rata adalah 44,0 minggu (min: 0,1, maks: 254,9) untuk lenalidomide / deksametason dan 23,1 minggu (min: 0,3, maks: 238,1) untuk plasebo / deksametason. Dalam kedua studi, tingkat respons lengkap (CR, respon lengkap), respon parsial (PR, respon parsial) dan respon keseluruhan (CR + PR) pada kelompok lenalidomide / deksametason tetap secara signifikan lebih tinggi daripada kelompok deksametason / plasebo. Kelangsungan hidup rata-rata secara keseluruhan dalam analisis tindak lanjut yang diperpanjang dari studi bersama adalah 164,3 minggu (95% CI: 145,1, 192,6) pada pasien yang diobati dengan lenalidomide / deksametason dibandingkan dengan 136,4 minggu (95% CI: 113,1, 161,7) pada pasien yang diobati dengan plasebo / deksametason Terlepas dari kenyataan bahwa 170 dari 351 pasien yang diacak untuk pengobatan plasebo / deksametason menerima terapi lenalidomide setelah perkembangan penyakit atau setelah kebutaan, analisis kelangsungan hidup keseluruhan yang dikumpulkan menunjukkan keuntungan kelangsungan hidup yang signifikan secara statistik untuk kelompok lenalidomide / deksametason dibandingkan dengan plasebo / kelompok deksametason (tingkat bahaya = 0,833, 95% CI = [0,687, 1,009], p = 0,045).
Tabel 7: Ringkasan hasil analisis kemanjuran pada tanggal batas untuk tindak lanjut yang diperpanjang - Studi bersama MM-009 dan MM-010 (tanggal batas masing-masing: 23 Juli 2008 dan 2 Maret 2008)
a: Analisis univariat dua sisi membandingkan kurva kelangsungan hidup antara kelompok perlakuan. b: Uji chi-kuadrat dua sisi dengan koreksi kontinuitas.
Sindrom mielodisplastik
Kemanjuran dan keamanan lenalidomide dievaluasi pada pasien dengan anemia yang bergantung pada transfusi karena sindrom myelodysplastic risiko rendah atau menengah-1 yang terkait dengan kelainan sitogenetik penghapusan 5q, dengan atau tanpa kelainan sitogenetik lainnya, dalam dua studi utama. : Fase III, multicenter , lenalidomide oral acak, double-blind, terkontrol plasebo, 3-lengan, dua dosis oral (10 mg dan 5 mg) versus studi plasebo (MDS-004); dan Fase II, multisenter, lengan tunggal, label terbuka, pada lenalidomide (10 mg) (MDS-003).
Hasil di bawah ini mewakili populasi niat-untuk-mengobati yang dipelajari di MDS-003 dan MDS-004; hasil untuk subpopulasi dengan penghapusan 5q terisolasi ditampilkan secara terpisah (lihat bagian 4.1 untuk indikasi yang disetujui).
Dalam studi MDS-004, di mana 205 pasien diacak sama untuk pengobatan dengan lenalidomide 10 mg, 5 mg atau plasebo, analisis efikasi primer terdiri dari membandingkan tingkat respons kemandirian transfusi pada kelompok lenalidomide 10 mg, dan 5 mg dibandingkan dengan plasebo lengan (fase double-blind 16-52 minggu dan fase label terbuka hingga total 156 minggu).Pada pasien yang tidak menunjukkan setidaknya respon eritroid ringan setelah 16 minggu, pengobatan dihentikan.Pasien yang memiliki bukti setidaknya respon eritroid ringan dapat melanjutkan terapi sampai kekambuhan eritroid, perkembangan penyakit, atau toksisitas yang tidak dapat diterima.setelah 16 minggu pengobatan mereka diizinkan untuk beralih dari plasebo ke 5 mg lenalidomide atau melanjutkan pengobatan dengan lenalidomide pada dosis yang lebih tinggi (5 mg sampai 10 mg).
Dalam studi MDS-003, di mana 148 pasien diobati dengan lenalidomide dengan dosis 10 mg, analisis efikasi primer terdiri dari evaluasi kemanjuran pengobatan lenalidomide dalam mencapai peningkatan hematopoietik pada subjek dengan sindrom myelodysplastic. 1.
Tabel 8: Ringkasan hasil efikasi - MDS-004 (fase double-blind) dan MDS-003, populasi yang ingin diobati
Subyek yang diobati dengan lenalidomide 10 mg pada 21 dari siklus 28 hari
Subyek yang diobati dengan lenalidomide 5 mg pada 28 dari siklus 28 hari
* Sebagian besar pasien dalam kelompok plasebo menghentikan pengobatan double-blind karena kurangnya kemanjuran setelah 16 minggu pengobatan, sebelum memasuki fase label terbuka
#Berhubungan dengan peningkatan Hgb sebesar 1 g/dL
Tidak tercapai (median tidak tercapai)
Dalam penelitian MDS-004, proporsi pasien dengan sindrom myelodysplastic yang secara signifikan lebih tinggi mencapai titik akhir primer kemandirian transfusi (> 182 hari) dengan lenalidomide 10 mg, dibandingkan dengan plasebo (55,1% vs 6,0%) Di antara 47 pasien dengan kelainan sitogenetik .
Del (5q) diisolasi dan diobati dengan 10 mg lenalidomide, 27 pasien (57,4%) mencapai kemandirian dari transfusi eritrosit.
Waktu rata-rata untuk kemandirian transfusi pada kelompok lenalidomide 10 mg adalah 4,6 minggu Durasi rata-rata kemandirian transfusi tidak tercapai di salah satu kelompok pengobatan, tetapi diharapkan melebihi 2 tahun untuk subyek yang diobati dengan lenalidomide. hemoglobin (Hgb) dari baseline pada kelompok 10 mg adalah 6,4 g / dL.
Titik akhir studi tambahan termasuk respon sitogenetik (respon sitogenetik mayor dan minor diamati pada 30,0% dan 24,0% subjek dalam kelompok 10 mg, masing-masing), penilaian kualitas hidup terkait kesehatan (HRQoL), dan perkembangan menjadi leukemia myeloid akut. Hasil dari respon sitogenetik dan HRQoL konsisten dengan hasil dari titik akhir primer dan mendukung pengobatan dengan lenalidomide daripada plasebo.
Dalam penelitian MDS-003, persentase tinggi pasien dengan sindrom myelodysplastic mencapai kemandirian transfusi (> 182 hari) dengan lenalidomide 10 mg (58,1%). Median waktu kemandirian transfusi adalah 4,1 minggu Median durasi kemandirian transfusi adalah 114,4 minggu Median peningkatan hemoglobin (Hgb) adalah 5,6 g/dl.
Respon sitogenetik mayor dan minor diamati pada masing-masing 40,9% dan 30,7% subjek.
Sebagian besar subjek yang terdaftar di MDS-003 (72,9%) dan MDS-004 (52,7%) sebelumnya telah diobati dengan agen perangsang eritropoiesis.
Limfoma sel mantel
Kemanjuran dan keamanan lenalidomide pada pasien dengan limfoma sel mantel dievaluasi dalam fase II, multisenter, acak, studi label terbuka versus pilihan penyelidik monoterapi pada pasien yang refrakter terhadap rejimen terakhir atau yang telah mengalami satu hingga tiga kekambuhan ( Studi MCL-002).
Pasien berusia minimal 18 tahun dengan limfoma sel mantel yang dikonfirmasi secara histologis dan penyakit terukur pada CT didaftarkan. Pasien harus telah menerima pengobatan sebelumnya yang memadai dengan setidaknya satu rejimen kemoterapi kombinasi sebelumnya. Selain itu, pasien diharuskan tidak memenuhi syarat untuk kemoterapi intensif dan / atau transplantasi pada inklusi penelitian. Pasien diacak 2: 1 untuk lenalidomide atau kelompok kontrol. Pilihan pengobatan penyelidik diputuskan sebelumnya. pengacakan dan terdiri dari monoterapi dengan klorambusil, sitarabin, rituximab, fludarabin atau gemcitabine.
Lenalidomide diberikan secara oral, dengan dosis 25 mg sekali sehari selama 21 hari pertama (G1 hingga G21) dari siklus 28 hari berulang sampai perkembangan atau toksisitas yang tidak dapat diterima. Pasien dengan gangguan ginjal sedang harus menerima dosis awal lenalidomide yang lebih rendah (10 mg per hari) dengan jadwal yang sama.
Demografi dasar sebanding antara lenalidomide dan kelompok kontrol. Kedua populasi pasien memiliki usia rata-rata 68,5 tahun, dengan rasio pasien laki-laki dan perempuan yang sebanding.Baik status kinerja ECOG dan jumlah terapi sebelumnya sebanding pada kedua kelompok.
Titik akhir kemanjuran utama dalam MCL-002 adalah kelangsungan hidup bebas perkembangan (PFS).
Hasil efikasi untuk populasi Intent-to-Treat (ITT) dinilai oleh Independent Review Commission (Komite Peninjau Independen, IRC) dan disajikan pada tabel di bawah ini.
Tabel 9: Ringkasan hasil kemanjuran - studi MCL-002, populasi niat untuk mengobati
CI = selang kepercayaan; CRR = tingkat respons lengkap; CR = tanggapan lengkap; CRu = tanggapan lengkap tidak dikonfirmasi; DMC = komite pemantau data; ITT = niat untuk mengobati; HR = rasio bahaya; KM = Kaplan-Meier; MIPI = Indeks Prognostik Internasional Limfoma Sel Mantel; NP = tidak relevan; ORR = tingkat respons keseluruhan; PD = penyakit progresif; PFS = kelangsungan hidup bebas perkembangan; PR = tanggapan parsial; SCT = transplantasi sel induk; SD = penyakit stabil; SE = kesalahan standar.
a Median didasarkan pada estimasi KM.
b Rentang dihitung sebagai 95% CI sehubungan dengan waktu kelangsungan hidup rata-rata.
e Mean dan median adalah statistik univariat tanpa koreksi pemotongan.
d Variabel stratifikasi termasuk waktu dari diagnosis hingga dosis pertama (
e Pengujian berurutan didasarkan pada rata-rata tertimbang dari statistik uji peringkat log, menggunakan uji peringkat log yang tidak distratifikasi untuk peningkatan ukuran sampel dan uji peringkat log yang tidak distratifikasi dari analisis primer. Bobot didasarkan pada peristiwa yang diamati pada tanggal pertemuan ketiga RCD dan didasarkan pada perbedaan antara peristiwa yang diamati dan peristiwa yang diharapkan pada saat analisis primer.
HR sekuensial terkait dan 95% CI yang sesuai disajikan.
Dalam studi MCL-002 pada populasi ITT, ada peningkatan kematian yang tampak secara keseluruhan dalam 20 minggu pada kelompok lenalidomide, 22/170 (13%), dibandingkan dengan 6/84 (7%) pada kelompok kontrol. Pada pasien dengan beban tumor yang tinggi, angka yang sesuai adalah 16/81 (20%) dan 2/28 (7%) (lihat bagian 4.4).
Populasi pediatrik
European Medicines Agency telah melepaskan kewajiban untuk menyerahkan hasil penelitian dengan Revlimid di semua subset populasi pediatrik untuk multiple myeloma, sindrom myelodysplastic dan limfoma sel mantel (lihat bagian 4.2 untuk informasi tentang " penggunaan pediatrik).
05.2 "Sifat farmakokinetik -
Lenalidomide memiliki atom karbon asimetris; oleh karena itu molekulnya ada dalam bentuk optik aktif S (-) dan R (+). Lenalidomide diproduksi sebagai campuran rasemat. Lenalidomide umumnya lebih larut dalam pelarut organik, tetapi menunjukkan kelarutan maksimum dalam larutan HCl 0,1N.
Penyerapan
Lenalidomide cepat diserap setelah pemberian oral pada sukarelawan sehat, dalam kondisi puasa, mencapai konsentrasi plasma maksimum antara 0,5 dan 2 jam setelah pemberian dosis. Pada pasien dan sukarelawan sehat konsentrasi maksimum (Cmax) dan l " area di bawah kurva konsentrasi-waktu ( AUC) meningkat secara proporsional dengan meningkatnya dosis. Dosis berulang tidak menyebabkan akumulasi obat yang signifikan. Dalam plasma, konsentrasi relatif dari S- dan R- enansiomer dari lenalidomide adalah sekitar 56% dan 44%, masing-masing.
Pemberian bersama makanan tinggi kalori dan tinggi lemak pada sukarelawan sehat mengurangi tingkat penyerapan, menghasilkan sekitar 20% penurunan area di bawah AUC dan 50% penurunan Cmax plasma. Namun, dalam studi pendaftaran sindrom multiple myeloma dan myelodysplastic penting di mana keamanan dan kemanjuran lenalidomide ditetapkan, obat diberikan tanpa pertimbangan asupan makanan. Oleh karena itu, lenalidomide dapat diberikan dengan atau tanpa makanan.
Analisis farmakokinetik populasi menunjukkan bahwa tingkat penyerapan lenalidomide oral serupa antara pasien dengan multiple myeloma, pasien dengan sindrom myelodysplastic dan pasien dengan limfoma sel mantel.
Distribusi
Secara invitro, Lenalidomide berlabel 14C memiliki ikatan yang buruk dengan protein plasma, dengan nilai rata-rata masing-masing 23% dan 29%, pada pasien dengan multiple myeloma dan sukarelawan sehat.
Lenalidomide hadir dalam air mani (
Biotransformasi dan eliminasi
Hasil studi metabolisme manusia yang dilakukan in vitro menunjukkan bahwa lenalidomide tidak dimetabolisme oleh enzim sitokrom P450, menunjukkan bahwa pemberian lenalidomide bersama dengan produk obat yang menghambat enzim sitokrom P450 tidak mungkin menghasilkan interaksi obat metabolik pada manusia. in vitro menunjukkan bahwa lenalidomide tidak memiliki efek penghambatan pada CYP1A2, CYP2C9, CYP2C19, CYP2D6, CYP2E1, CYP3A atau UGT1A1. Oleh karena itu, lenalidomide tidak mungkin menyebabkan interaksi obat yang relevan secara klinis bila diberikan bersamaan dengan substrat enzim ini.
Pendidikan in vitro menunjukkan bahwa lenalidomide bukanlah substrat dari human breast cancer resistance protein (BCRP), transporter multidrug resistance protein (MRP) MRP1, MRP2 atau MRP3, organic anion transporter (OAT) OAT1 dan OAT3, polypeptide organic anion transporter (OATP) OATP1B1, organic pengangkut kation (OCT) OCT1 dan OCT2, protein ekstrusi obat dan toksin (MATE) MATE1 dan pengangkut kation organik baru (OCTN) OCTN1 dan OCTN2.
Pendidikan in vitro menunjukkan bahwa lenalidomide tidak memiliki efek penghambatan pada pompa ekspor garam empedu manusia (BSEP), BCRP, MRP2, OAT1, OAT3, OATP1B1, OATP1B3 dan OCT2.
Sebagian besar lenalidomide dieliminasi melalui ekskresi urin.Kontribusi ekskresi ginjal terhadap total klirens pada subjek dengan fungsi ginjal normal adalah 90%, sedangkan 4% lenalidomide dieliminasi melalui feses.
Lenalidomide dimetabolisme dengan buruk, sehingga 82% dari dosis diekskresikan tidak berubah dalam urin.Hydroxy-lenalidomide dan N-acetyl-lenalidomide masing-masing sebesar 4,59% dan 1,83% dari dosis yang diekskresikan. Klirens lenalidomide ginjal melebihi laju filtrasi glomerulus, oleh karena itu setidaknya sampai batas tertentu disekresikan secara aktif.
Pada dosis 5 hingga 25 mg / hari, waktu paruh plasma sekitar 3 jam pada sukarelawan sehat dan berkisar antara 3 hingga 5 jam pada pasien dengan multiple myeloma, sindrom myelodysplastic atau limfoma sel mantel.
pasien lanjut usia
Tidak ada studi klinis khusus yang dilakukan untuk mengevaluasi farmakokinetik lenalidomide pada pasien usia lanjut. Analisis farmakokinetik populasi termasuk pasien berusia 39 hingga 85 tahun dan menunjukkan bahwa usia tidak mempengaruhi pembersihan (konsentrasi plasma) lenalidomide. Karena pasien lanjut usia lebih cenderung mengalami penurunan fungsi ginjal, disarankan agar Perhatian harus dilakukan dalam pemilihan dosis dan pemantauan fungsi ginjal disarankan sebagai tindakan pencegahan.
Gagal ginjal
Farmakokinetik lenalidomide dipelajari pada subjek dengan insufisiensi ginjal yang disebabkan oleh penyakit non-ganas. Dalam penelitian ini, dua metode digunakan untuk klasifikasi fungsi ginjal: klirens kreatinin urin diukur selama 24 jam dan klirens kreatinin diperkirakan dengan rumus Cockcroft-Gault.Hasil menunjukkan bahwa, dengan penurunan fungsi ginjal (waktu paruh lenalidomide meningkat dari kurang lebih 3,5 jam pada subjek dengan klirens kreatinin > 50 ml/menit hingga lebih dari 9 jam pada subjek dengan gangguan fungsi ginjal
Insufisiensi hati
Analisis farmakokinetik populasi termasuk pasien dengan insufisiensi hati ringan (N = 16, bilirubin total> 1 hingga 1,5 x ULN (Batas Normal) atau AST> ULN) dan menunjukkan bahwa "insufisiensi hati ringan tidak mempengaruhi pembersihan (konsentrasi plasma) lenalidomide Tidak ada data yang tersedia pada pasien dengan gangguan hati sedang sampai berat.
Faktor intrinsik lainnya
Analisis farmakokinetik populasi menunjukkan bahwa berat badan (33-135 kg), jenis kelamin, ras dan jenis keganasan hematologis (MM, MDS atau MCL) tidak memiliki efek yang relevan secara klinis pada pembersihan lenalidomide pada pasien dewasa.
05.3 Data keamanan praklinis -
Sebuah studi perkembangan embrio-janin dilakukan pada monyet yang diobati dengan lenalidomide dengan dosis mulai dari 0,5 hingga 4 mg / kg / hari. Hasil penelitian ini menunjukkan bahwa lenalidomide menyebabkan malformasi eksternal termasuk lubang anus yang tidak paten dan malformasi ekstremitas atas dan bawah (bagian ekstremitas yang melengkung, memendek, malformasi, malrotasi dan/atau tidak ada, oligo dan/atau polidaktili) pada keturunan monyet betina yang menerima obat selama kehamilan.
Efek visceral yang berbeda juga telah diamati pada masing-masing janin (perubahan warna, fokus merah di berbagai organ, massa kecil tidak berwarna di atas katup atrioventrikular, kantong empedu kecil, diafragma cacat).
Lenalidomide menunjukkan potensi risiko toksisitas akut; pada hewan pengerat, dosis mematikan minimal setelah pemberian oral adalah> 2.000 mg / kg / hari. Pemberian oral berulang 75, 150 dan 300 mg / kg / hari hingga 26 minggu menghasilkan peningkatan mineralisasi pelvis ginjal terkait pengobatan reversibel pada tikus, terutama betina, pada semua tingkat dosis. Tingkat tidak ada efek samping yang dapat diamati (NOAEL, tidak ada tingkat efek samping yang diamati) dianggap kurang dari 75 mg / kg / hari, dan kira-kira 25 kali lebih besar dari paparan harian manusia berdasarkan nilai AUC. Pada monyet, pemberian oral berulang 4 dan 6 mg / kg / hari untuk periode hingga 20 minggu menghasilkan kematian dan toksisitas yang signifikan (penurunan berat badan yang nyata, penurunan sel darah putih, jumlah sel darah merah dan trombosit, perdarahan di beberapa organ, radang selaput lendir). saluran pencernaan, atrofi jaringan limfatik dan sumsum tulang). Juga pada monyet, pemberian oral berulang 1 dan 2 mg / kg / hari, untuk periode hingga 1 tahun, menghasilkan perubahan reversibel dalam seluleritas sumsum tulang, sedikit pengurangan rasio sel myelo-erythroid dan atrofi timus. Sedikit penurunan jumlah sel darah putih diamati hingga 1 mg / kg / hari, yang sesuai dengan dosis yang kira-kira sama pada manusia, berdasarkan perbandingan AUC.
Studi mutagenisitas dilakukan in vitro (mutasi bakteri, limfosit manusia, limfoma murine, transformasi menjadi sel embrio hamster Syria) dan in vivo (uji mikronukleus tikus) tidak mengungkapkan efek terkait obat apa pun baik pada tingkat gen maupun pada tingkat kromosom. Studi karsinogenisitas belum dilakukan dengan lenalidomide.
Toksisitas perkembangan sebelumnya telah dipelajari pada kelinci. Pada penelitian ini kelinci diberikan lenalidomide 3, 10 dan 20 mg/kg/hari per oral. Absennya lobus intermediet paru diamati pada dosis 10 dan 20 mg/kg/hari, berkorelasi dengan dosis, dan ginjal ektopik pada dosis 20 mg/kg/hari. 20 mg / kg / hari.dosis beracun bagi ibu, mereka mungkin disebabkan oleh efek langsung Pada dosis 10 dan 20 mg / kg / hari, perubahan jaringan lunak dan kerangka juga telah diamati pada janin.
06.0 INFORMASI FARMASI -
06.1 Eksipien -
Isi kapsul
Laktosa anhidrat
Selulosa mikrokristalin
Natrium kroskarmelosa
Magnesium Stearate
Cangkang kapsul
Jeli
Titanium dioksida (E171)
Indigo carmine (E132)
Oksida besi kuning (E172)
Tinta kata-kata
Lak
Propilen glikol
Oksida besi hitam (E172)
Potasium hidroksida
06.2 Ketidakcocokan "-
Tidak berhubungan.
06.3 Masa berlaku "-
3 tahun.
06.4 Tindakan pencegahan khusus untuk penyimpanan -
Obat ini tidak memerlukan kondisi penyimpanan khusus.
06.5 Sifat kemasan langsung dan isi kemasan -
Polyvinyl chloride (PVC) / polychlorotrifluoroethylene (PCTFE) / aluminium foil blister berisi 7 kapsul keras.
Kemasan 21 kapsul.
06.6 Petunjuk penggunaan dan penanganan -
Obat yang tidak terpakai dan limbah yang berasal dari obat ini harus dibuang sesuai dengan peraturan setempat.
07.0 PEMEGANG "OTORISASI PEMASARAN" -
Celgene Eropa Terbatas
1 Jalan Panjang
Taman Stockley
Jembatan Ux
UB11 1DB
Inggris
08.0 NOMOR OTORITAS PEMASARAN -
UE / 1/07/391/002
038016022
09.0 TANGGAL OTORISASI PERTAMA ATAU PEMBARUAN OTORISASI -
Tanggal otorisasi pertama: 14 Juni 2007
Tanggal pembaruan terakhir: 14 Juni 2012
10.0 TANGGAL REVISI TEKS -
D.CCE September 2016
11.0 UNTUK RADIOFarmasi, DATA LENGKAP PADA DOSIMETRI RADIASI INTERNAL -
12.0 UNTUK OBAT RADIO, PETUNJUK LEBIH LANJUT TENTANG PERSIAPAN EKSTEMPORER DAN PENGENDALIAN KUALITAS -