Bahan aktif: Atosiban
Tractocile 6,75 mg / 0,9 ml larutan untuk injeksi
Sisipan paket traktosil tersedia untuk ukuran paket:- Tractocile 6,75 mg / 0,9 ml larutan untuk injeksi
- Tractocile 37,5 mg / 5 ml konsentrat untuk larutan infus
Mengapa Traktosil digunakan? Untuk apa?
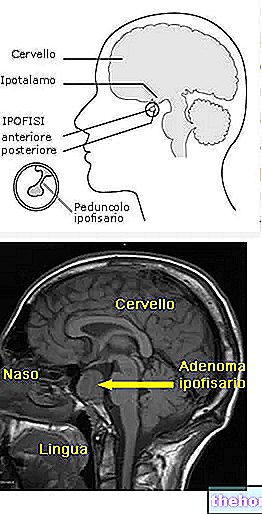
Traktosil mengandung atosiban. Tractocile dapat digunakan untuk menunda kelahiran prematur bayi Anda. Tractocile digunakan pada wanita dewasa yang hamil antara minggu ke-24 dan ke-33 kehamilan.
Traktosil bekerja dengan mengurangi intensitas kontraksi rahim, juga memperlambat frekuensi kontraksi, dengan menghalangi efek hormon alami dalam tubuh yang disebut "oksitosin" yang menyebabkan kontraksi rahim.
Kontraindikasi Ketika Tractocile tidak boleh digunakan
Jangan gunakan Traktosil:
- jika Anda telah hamil kurang dari 24 minggu
- jika Anda telah hamil lebih dari 33 minggu
- jika Anda mengalami kerusakan air (ketuban pecah dini) setelah minggu ke-30 kehamilan
- jika janin memiliki detak jantung yang tidak normal
- jika Anda mengalami "pendarahan vagina yang, menurut penilaian dokter, membutuhkan pengiriman segera"
- jika Anda memiliki kondisi yang disebut 'pre-eklampsia berat' yang, menurut penilaian dokter, memerlukan persalinan segera. Pre-eklampsia berat adalah suatu kondisi di mana Anda memiliki tekanan darah tinggi, retensi cairan dan / atau adanya protein dalam urin
- jika Anda memiliki kondisi yang disebut "eklampsia" yang mirip dengan "pre-eklampsia berat" tetapi dengan tambahan kejang. Kondisi ini membutuhkan persalinan segera
- dalam kasus kematian janin
- jika Anda memiliki atau diduga mengalami "infeksi rahim" - jika plasenta menutupi jalan lahir
- dalam kasus pelepasan plasenta dari dinding rahim
- dalam kondisi lain apa pun bagi Anda atau janin yang membahayakan kelanjutan kehamilan
- jika Anda alergi terhadap atosiban atau salah satu bahan lain dari obat ini (tercantum di bagian 6).
Jangan gunakan Tractocile jika Anda berada dalam salah satu kondisi yang dijelaskan di atas. Jika Anda tidak yakin, tanyakan kepada dokter, bidan atau apoteker Anda sebelum menggunakan Tractocile.
Kewaspadaan penggunaan Apa yang perlu Anda ketahui sebelum menggunakan Tractocile
Bicaralah dengan dokter, bidan atau apoteker Anda sebelum menggunakan Tractocile:
- jika Anda mengira Anda mengalami ketuban pecah dini (ketuban pecah dini)
- jika Anda menderita masalah ginjal atau hati
- jika kehamilan antara minggu ke-24 dan ke-27
- jika kehamilannya multipel
- jika kontraksi berulang, pengobatan dengan Tractocile dapat diulang 3 kali lagi
- jika janin kecil dibandingkan dengan tahap kehamilan
- setelah melahirkan, rahim mungkin memiliki kapasitas yang berkurang untuk berkontraksi. Hal ini dapat menyebabkan perdarahan
- jika Anda sedang hamil anak kembar dan/atau sedang mengonsumsi obat-obatan yang dapat menunda kelahiran bayi Anda, seperti obat-obatan yang digunakan untuk tekanan darah tinggi. Kondisi tersebut dapat meningkatkan risiko terjadinya edema paru (penumpukan cairan di paru-paru).
Jika Anda memiliki salah satu kondisi yang dijelaskan di atas, atau jika Anda tidak yakin, bicarakan dengan dokter, bidan, atau apoteker Anda sebelum menggunakan Tractocile.
Anak-anak dan remaja
Tractocile belum diteliti pada wanita hamil di bawah usia 18 tahun.
Interaksi Obat atau makanan mana yang dapat mengubah efek Tractocile?
Beri tahu dokter, bidan, atau apoteker Anda jika Anda sedang mengonsumsi, baru saja mengonsumsi atau mungkin sedang mengonsumsi obat lain, bahkan yang tidak diresepkan, termasuk obat herbal.
Peringatan Penting untuk diketahui bahwa:
Kehamilan dan menyusui
Jika Anda sedang hamil atau menyusui untuk kelahiran sebelumnya, Anda harus berhenti menyusui saat dirawat dengan Tractocile.
Dosis, Cara dan Waktu Pemberian Cara Pemakaian Tractocile : Posology
Tractocile adalah obat untuk penggunaan di rumah sakit saja, yang hanya boleh diberikan oleh dokter, perawat atau bidan Anda. Mereka akan menentukan jumlah yang dibutuhkan untuk Anda dan memastikan larutannya jernih, tanpa partikel.
Tractocile diberikan ke dalam vena (intravena) dalam tiga tahap berturut-turut:
- Injeksi intravena awal 6,75 mg dalam 0,9 ml secara perlahan disuntikkan ke dalam vena selama satu menit.
- Selanjutnya, infus kontinu (tetes) dengan dosis 18 mg / jam diberikan selama 3 jam.
- Selanjutnya diberikan infus kontinyu (drip) dengan dosis 6 mg/jam selama maksimal 45 jam, atau sampai kontraksi uterus berhenti.
Total durasi pengobatan tidak boleh lebih dari 48 jam.
Kursus pengobatan lebih lanjut dengan Tractocile dapat digunakan jika kontraksi berulang. Perawatan traktosil dapat diulang tiga kali lagi.
Selama perawatan dengan Tractocile, kontraksi dan detak jantung janin dapat dipantau.
Direkomendasikan bahwa tidak lebih dari tiga pengobatan lebih lanjut diberikan selama kehamilan.
Efek Samping Apa efek samping dari Tractocile?
Seperti semua obat-obatan, obat ini dapat menyebabkan efek samping, meskipun tidak semua orang mendapatkannya. Efek yang tidak diinginkan yang diamati pada ibu umumnya kecil. Tidak ada efek yang tidak diinginkan yang diketahui pada janin atau neonatus.
Berikut ini adalah efek samping yang mungkin terjadi dengan penggunaan obat ini:
Sangat umum (terjadi pada lebih dari 1 dari 10 orang)
- Malaise (mual)
Umum (terjadi pada kurang dari 1 dari 10 orang)
- Sakit kepala
- Pusing
- Siram
- Merasa sakit (muntah)
- Percepatan detak jantung
- Menurunkan tekanan darah. Gejala mungkin termasuk pusing atau pusing
- Reaksi tempat injeksi
- Peningkatan nilai gula darah
Jarang (terjadi pada kurang dari 1 dari 100 orang)
- Suhu tinggi (demam)
- Sulit tidur (insomnia)
- Gatal
- Ruam kulit
Langka (terjadi pada kurang dari 1 dari 1.000 orang)
- Kurangnya kemampuan rahim untuk berkontraksi setelah melahirkan, hal ini dapat menyebabkan perdarahan
- Reaksi alergi
Anda mungkin mengalami kesulitan bernapas atau edema paru (penumpukan cairan di paru-paru), terutama jika Anda hamil kembar dan/atau sedang mengonsumsi obat-obatan lain yang dapat menunda kelahiran bayi Anda, seperti obat-obatan yang digunakan untuk tekanan darah tinggi.
Jika Anda mendapatkan efek samping, bicarakan dengan dokter, bidan atau perawat Anda, termasuk kemungkinan efek samping yang tidak tercantum dalam brosur ini.
Kadaluwarsa dan Retensi
Jauhkan obat ini dari pandangan dan jangkauan anak-anak.
Jangan gunakan obat ini setelah tanggal kadaluwarsa yang tertera pada karton setelah EXP {MM / YYYY}
Tanggal kedaluwarsa mengacu pada hari terakhir bulan itu.
Simpan di lemari es (2°C - 8°C).
Simpan dalam kemasan aslinya untuk melindungi dari cahaya. Larutan encer untuk pemberian intravena harus digunakan dalam waktu 24 jam setelah persiapan.
Jangan gunakan obat ini jika Anda melihat ada partikel dan perubahan warna.
Informasi lainnya
Apa isi Traktosil?
- Bahan aktifnya adalah atosiban.
- Setiap vial Tractocile 6,75 mg / 0,9 ml larutan injeksi mengandung atosiban asetat, setara dengan 6,75 mg atosiban dalam 0,9 ml.
- Bahan lainnya adalah: manitol, asam klorida dan air untuk suntikan.
Seperti apa Traktosil dan isi paketnya
Tractocile 6,75 mg / 0,9 ml larutan untuk injeksi adalah larutan bening, tidak berwarna, bebas partikel.
Satu bungkus berisi satu botol berisi 0,9 ml larutan.
Informasi berikut ini ditujukan untuk profesional kesehatan saja
Instruksi untuk penggunaan
Sebelum menggunakan Tractocile, larutan harus diperiksa untuk memastikannya jernih dan bebas dari partikel. Tractocile diberikan secara intravena dalam 3 tahap berturut-turut:
- Injeksi intravena awal 6,75 mg dalam 0,9 ml secara perlahan disuntikkan ke dalam vena selama satu menit.
- Setelah itu, infus kontinu dengan dosis 24 ml / jam diberikan selama 3 jam.
- Selanjutnya diberikan infus kontinyu dengan dosis 8 ml/jam sampai dengan 45 jam, atau sampai kontraksi uterus mereda.
Total durasi pengobatan tidak boleh lebih dari 48 jam. Kursus pengobatan lebih lanjut dengan Tractocile dapat digunakan jika kontraksi berulang. Dianjurkan untuk tidak melakukan lebih dari 3 kursus perawatan lebih lanjut selama kehamilan.
Sumber Paket Leaflet: AIFA (Badan Obat Italia). Konten yang diterbitkan pada Januari 2016. Informasi yang ada mungkin tidak up-to-date.
Untuk memiliki akses ke versi terbaru, disarankan untuk mengakses situs web AIFA (Badan Obat Italia). Penafian dan informasi yang berguna.
01.0 NAMA PRODUK OBAT
TRAKTOSIL 6.75 MG / 0.9 ML SOLUSI UNTUK INJEKSI
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF
Setiap botol 0,9 ml larutan mengandung 6,75 mg atosiban (sebagai asetat).
Untuk daftar lengkap eksipien, lihat bagian 6.1.
03.0 FORMULIR FARMASI
Solusi untuk injeksi (persiapan injeksi).
Jelas, solusi tidak berwarna, tanpa bukti partikel.
04.0 INFORMASI KLINIS
04.1 Indikasi Terapi
TRACTOCILE diindikasikan untuk menunda kelahiran prematur yang akan datang pada pasien dewasa hamil dengan:
- Kontraksi uterus teratur berlangsung minimal 30 detik dengan frekuensi 4 setiap 30 menit
- dilatasi serviks dari 1 hingga 3 cm (0-3 untuk nulipara) dan hilangnya leher rahim 50%
- usia kehamilan dari 24 hingga 33 minggu penuh
- Detak jantung janin normal
04.2 Posologi dan cara pemberian
Perawatan dengan TRACTOCILE harus dimulai dan dilanjutkan oleh dokter yang berspesialisasi dalam perawatan persalinan prematur.
TRACTOCILE diberikan secara intravena dalam 3 tahap berturut-turut: dosis bolus awal (6,75 mg), disiapkan dengan larutan TRACTOCILE 6,75 mg / 0,9 ml untuk injeksi, diikuti segera dengan infus kontinu dosis tinggi (beban infus 300 mcg / menit) TRACTOCILE 37,5 mg / 5 ml konsentrat untuk larutan infus intravena selama 3 jam dan selanjutnya dengan dosis yang lebih rendah dari TRACTOCILE 37,5 mg / 5 ml konsentrat untuk larutan infus intravena (infus selanjutnya 100 mcg / menit) untuk jangka waktu maksimum 45 jam. Durasi perawatan tidak boleh lebih dari 48 jam. Dosis total yang diberikan selama terapi penuh TRACTOCILE biasanya tidak boleh melebihi 330,75 mg atosiban.
Terapi intravena dengan injeksi bolus awal harus dimulai sesegera mungkin, segera setelah diagnosis persalinan prematur dibuat.Setelah pemberian bolus dilakukan, lanjutkan dengan infus (lihat Ringkasan Karakteristik Produk TRACTOCILE 37,5 mg / 5 ml konsentrat untuk larutan infus). Jika kontraksi uterus berlanjut selama pengobatan dengan TRACTOCILE, terapi alternatif harus dipertimbangkan.
Tidak ada pengalaman pengobatan dengan atosiban pada pasien dengan gangguan fungsi hati atau ginjal. Tidak ada penyesuaian dosis yang diantisipasi pada insufisiensi ginjal karena hanya sejumlah kecil atosiban yang diekskresikan dalam urin.Pada pasien dengan insufisiensi hati, atosiban harus digunakan dengan hati-hati.
Tabel berikut menunjukkan posologi lengkap injeksi bolus diikuti dengan infus:
Perawatan selanjutnya
Jika pengobatan selanjutnya dengan atosiban diperlukan, administrasi bolus TRACTOCILE 6,75 mg / 0,9 ml, larutan injeksi harus dimulai lagi, diikuti dengan infus dengan TRACTOCILE 37,5 mg / 5 ml, konsentrat untuk larutan infus intravena.
04.3 Kontraindikasi
TRAKTOSIL tidak boleh diberikan dalam kondisi berikut:
- Usia kehamilan di bawah 24 atau di atas 33 minggu penuh
- Ketuban pecah dini pada usia kehamilan lebih dari 30 minggu
- Detak jantung janin yang tidak normal
- Pendarahan rahim pra-kelahiran yang membutuhkan pelahiran segera
- Eklampsia dan preeklamsia berat yang membutuhkan persalinan
- Kematian janin intrauterin
- Dugaan infeksi intrauterin
- Plasenta previa
- Solusio plasenta
- Kondisi lain dari ibu atau janin di mana kelanjutan kehamilan berbahaya
- Diketahui hipersensitivitas terhadap zat aktif atau salah satu eksipien.
04.4 Peringatan khusus dan tindakan pencegahan yang tepat untuk digunakan
Ketika atosiban digunakan pada pasien yang kemungkinan ketuban pecah dini tidak dapat disingkirkan, manfaat dari keterlambatan persalinan dan setiap risiko dari korionamnionitis harus dipertimbangkan.
Tidak ada pengalaman pengobatan dengan atosiban pada pasien dengan gangguan fungsi hati atau ginjal. Tidak ada penyesuaian dosis yang diantisipasi pada insufisiensi ginjal karena hanya sejumlah kecil atosiban yang diekskresikan dalam urin.Pada pasien dengan insufisiensi hati, atosiban harus digunakan dengan hati-hati (lihat bagian 4.2 dan 5.2).
Hanya ada sedikit pengalaman klinis mengenai pemberian atosiban pada kehamilan ganda atau pada kelompok usia kehamilan 24-27 minggu karena sejumlah kecil pasien yang menjalani pengobatan. Oleh karena itu, manfaat atosiban dalam subkelompok ini tidak pasti.
Perawatan selanjutnya dengan TRACTOCILE dimungkinkan, tetapi pengalaman klinis untuk beberapa perawatan berikutnya dibatasi hingga maksimal 3 program perawatan lebih lanjut (lihat bagian 4.2).
Jika terjadi retardasi pertumbuhan intrauterin, keputusan untuk melanjutkan atau memulai kembali pengobatan dengan TRACTOCILE tergantung pada penentuan maturitas janin.
Kontraksi uterus dan denyut jantung janin harus dipantau selama pemberian atosiban dan jika terjadi kontraksi uterus yang persisten.
Atosiban, sebagai antagonis oksitosin, secara teoritis dapat menyebabkan relaksasi uterus dan kehilangan darah postpartum, sehingga kehilangan darah postpartum harus dikontrol.
Namun, kontraksi uterus postpartum yang tidak memadai tidak ditemukan dalam uji klinis.
04.5 Interaksi dengan produk obat lain dan bentuk interaksi lainnya
Atosiban tidak mungkin terlibat dalam interaksi obat yang dimediasi sitokrom P450 sejak penelitian in vitro menunjukkan bahwa atosiban tidak mewakili substrat untuk sistem sitokrom P450 dan tidak menghambat sistem enzim sitokrom P450 yang bertanggung jawab untuk metabolisme obat.
Studi interaksi dilakukan dengan labetalol dan betametason pada wanita sukarelawan yang sehat. Tidak ada interaksi klinis yang relevan yang diamati antara atosiban dan betametason atau labetalol.
04.6 Kehamilan dan menyusui
Pengobatan dengan atosiban hanya boleh digunakan ketika persalinan prematur telah didiagnosis antara minggu ke-24 dan ke-33 kehamilan lengkap. Jika selama kehamilan wanita tersebut sudah menyusui untuk kelahiran sebelumnya, menyusui harus dihentikan selama pengobatan dengan TRACTOCILE, karena pelepasan oksitosin selama menyusui dapat meningkatkan kontraktilitas uterus dan dengan demikian melawan efek terapi tokolitik.
Hasil studi klinis dengan atosiban mengungkapkan tidak ada efek pada laktasi.Sejumlah kecil atosiban berpindah dari plasma ke ASI ibu.
Hasil studi toksisitas embrio-janin tidak mengungkapkan efek toksik atosiban. Studi yang mengacu pada kapasitas reproduksi dan perkembangan embrio awal belum pernah dilakukan (lihat bagian 5.3).
04.7 Efek pada kemampuan mengemudi dan menggunakan mesin
Tidak berhubungan.
04.8 Efek yang tidak diinginkan
Dalam studi klinis, kemungkinan reaksi merugikan yang terkait dengan penggunaan atosiban diamati pada ibu. Secara total, 48% pasien yang diobati dengan atosiban mengalami reaksi merugikan selama studi klinis. Reaksi merugikan yang diamati umumnya ringan. Reaksi merugikan yang paling sering dilaporkan oleh ibu adalah mual (14%).
Pada bayi baru lahir, studi klinis tidak mengungkapkan reaksi merugikan spesifik akibat atosiban. Reaksi merugikan yang diamati pada bayi berada dalam kisaran normal dan insidennya sebanding dengan yang terlihat pada kelompok plasebo dan beta-mimetik.
Frekuensi reaksi merugikan yang tercantum di bawah ini ditentukan dengan menggunakan konvensi berikut: Sangat umum (≥ 1/10); umum (≥ 1/100,
04.9 Overdosis
Kasus overdosis atosiban yang jarang telah dilaporkan, terjadi tanpa tanda atau gejala tertentu. Tidak ada perawatan khusus yang diketahui dalam kasus overdosis.
05.0 SIFAT FARMAKOLOGIS
05.1 Sifat farmakodinamik
Kelompok farmakoterapi: ginekologi lainnya, kode ATC: G02CX01
TRACTOCILE mengandung atosiban (INN), peptida sintetis ([Mpa1, D-Tyr (Et) 2, Thr4, Orn8] -oxytocin) antagonis kompetitif oksitosin manusia pada tingkat reseptor.Hasil penelitian pada tikus dan marmut menunjukkan bahwa atosiban mengikat reseptor oksitosin untuk mengurangi frekuensi kontraksi dan tonus otot rahim, sehingga terjadi penekanan kontraksi rahim. Kemampuan atosiban untuk mengikat reseptor vasopresin, sehingga menghambat efek vasopresin itu sendiri, juga ditemukan.Pada hewan, atosiban tidak menunjukkan efek kardiovaskular.
Pada persalinan prematur manusia, atosiban, pada dosis yang dianjurkan, menghambat kontraksi uterus dan menginduksi ketenangan uterus. Efek relaksasi uterus cepat terbentuk setelah pemberian atosiban dan kontraksi berkurang secara signifikan dalam 10 menit untuk kemudian mencapai ketenangan uterus yang stabil (≤ 4 kontraksi / jam) selama 12 jam.
Uji klinis fase III (studi CAP-001) dilakukan pada 742 wanita yang didiagnosis dengan persalinan prematur antara minggu ke-23-33 kehamilan; penelitian ini melibatkan pasien yang diberikan secara acak atosiban (sesuai dengan jadwal pemberian dosis yang ditunjukkan) atau? -agonis (pada dosis yang dititrasi).
Titik akhir primer: Titik akhir utama untuk mengevaluasi kemanjuran produk adalah persentase pasien yang tidak melahirkan dalam 7 hari pertama sejak awal pengobatan dan tidak memerlukan pengobatan dengan tokolitik alternatif Data menunjukkan bahwa 59,6 % (n = 201) dan 47,7% (n = 163) dari pasien yang diobati dengan atosiban dan a?-agonis (p = 0,0004), masing-masing, tidak melahirkan dan tidak meminta pengobatan dengan tokolitik alternatif. Sebagian besar kegagalan yang tercatat dalam studi CAP-001 disebabkan oleh tolerabilitas yang rendah. Kegagalan pengobatan karena kemanjuran yang tidak mencukupi secara signifikan (p = 0,0003) lebih sering terjadi pada pasien yang diobati dengan atosiban (n = 48, 14,2%) dibandingkan pada pasien yang diobati dengan? -Agonist (n = 20, 5,8%).
Dalam studi CAP-001, kemungkinan tidak melahirkan dan tidak memerlukan tokolitik alternatif dalam 7 hari setelah memulai pengobatan serupa pada pasien yang diobati dengan atosiban dan beta-mimetik selama minggu ke-24-28 kehamilan.Namun, hasil ini didasarkan pada sampel yang sangat kecil (n = 129 pasien).
Enpoint Sekunder: Parameter efikasi sekunder termasuk persentase pasien yang tidak melahirkan dalam waktu 48 jam setelah memulai pengobatan.Mengenai parameter ini, tidak ada perbedaan antara kelompok atosiban dan beta-mimetik.
Rata-rata (SD) usia kehamilan saat melahirkan adalah serupa pada 2 kelompok: 35,6 dan 35,3 minggu untuk atosiban dan a? -Agonist kelompok, masing-masing (p = 0,37) Neonatal Intensive Care (CIN) serupa untuk kedua kelompok perlakuan (kurang lebih 30%), demikian pula data rawat inap dan data terapi ventilasi.Rerata (SD) berat lahir adalah 2491 gram pada kelompok yang diberi atosiban dan 2461 gram pada kelompok yang diberi?-agonis (p = 0,58).
Tampaknya tidak ada perbedaan dalam hasil janin dan ibu antara kelompok atosiban dan? -Agonist, tetapi uji klinis tidak cukup besar untuk mengesampingkan kemungkinan perbedaan.
Dari 361 wanita yang menerima pengobatan atosiban dalam studi fase III, 73 menjalani setidaknya satu pengobatan berikutnya, 8 menjalani setidaknya 2 pengobatan berikutnya, dan 2 menerima 3 pengobatan berikutnya (lihat bagian 4.4).
Karena keamanan dan kemanjuran atosiban pada wanita dengan usia kehamilan kurang dari 24 minggu penuh belum ditetapkan dalam uji coba terkontrol secara acak, pengobatan dengan atosiban pada kelompok pasien ini tidak dianjurkan (lihat bagian 4.3).
Dalam studi terkontrol plasebo, jumlah kematian janin/bayi adalah 5/295 (1,7%) pada kelompok plasebo dan 15/288 (5,2%) pada kelompok atosiban. Dari jumlah tersebut, 2 terjadi pada usia 5 dan 8 bulan. Sebelas dari lima belas kematian yang terdeteksi pada kelompok atosiban terkait dengan kehamilan dengan usia kehamilan antara minggu ke-20 dan ke-24. Perlu dicatat bahwa distribusi wanita berusia kurang dari 24 minggu tidak homogen (19 pada kelompok atosiban dan 4 pada kelompok plasebo).
Tidak ada perbedaan angka kematian pada wanita di atas usia kehamilan 24 minggu (1,7% pada kelompok plasebo dan 1,5% pada kelompok atosiban).
05.2 Sifat farmakokinetik
Konsentrasi plasma keadaan stabil, dinilai dengan infus atosiban (10 hingga 300 mcg / menit selama 12 jam) pada subjek sehat yang tidak hamil, meningkat sebanding dengan dosis yang diberikan.
Klirens, volume distribusi dan waktu paruh ditemukan tidak tergantung pada dosis yang diberikan.
Infus atosiban (300 mcg / menit selama periode 6-12 jam) pada wanita hamil dengan persalinan prematur menghasilkan konsentrasi plasma yang stabil dicapai dalam waktu 1 jam setelah dimulainya infus (nilai rata-rata 442 ± 73 ng / mL, dengan kisaran 298-533 ng / mL).
Pada akhir infus, konsentrasi plasma turun dengan cepat dengan waktu paruh awal (T?) dan akhir (T?) masing-masing 0,21 ± 0,01 dan 1,7 ± 0,3 jam. Nilai izin rata-rata adalah 41,8 ± 8,2 liter / jam. Rata-rata volume distribusi adalah 18,3 ± 6,8 liter.
Pada ibu hamil, atosiban 46-48% terikat pada protein plasma. Tidak diketahui apakah fraksi bebas di kompartemen ibu berbeda secara substansial dari fraksi janin. Atosiban tidak terdistribusi dalam sel darah merah.
Atosiban melewati penghalang plasenta. Setelah infus 300 mcg / menit pada wanita hamil yang sehat, rasio konsentrasi atosiban janin / ibu adalah 0,12.
2 metabolit telah diidentifikasi dalam plasma dan urin subjek manusia Rasio konsentrasi plasma metabolit utama M1 (des- (Orn8, Gly-NH2 9) - [Mpa1, D-Tyr (Et) 2, Thr4] - oksitosin) dan atosiban masing-masing adalah 1,4 dan 2,8 pada jam kedua dan pada akhir infus.
Tidak diketahui apakah M1 terakumulasi dalam jaringan. Kehadiran atosiban telah ditemukan dalam urin hanya dalam jumlah kecil dan konsentrasi urinnya kira-kira 50 kali lebih rendah daripada M1. Persentase atosiban yang diekskresikan dalam tinja tidak diketahui. Metabolit utama M1 kira-kira 10 kali lebih kuat dalam menghambat daripada atosiban in vitro kontraksi uterus yang diinduksi oleh oksitosin. Metabolit M1 diekskresikan dalam susu (lihat bagian 4.6).
Tidak ada pengalaman pengobatan dengan atosiban pada pasien dengan gangguan fungsi hati atau ginjal. Tidak ada penyesuaian dosis yang diantisipasi pada insufisiensi ginjal karena hanya sejumlah kecil atosiban yang diekskresikan dalam urin.Pada pasien dengan insufisiensi hati, atosiban harus digunakan dengan hati-hati (lihat bagian 4.2 dan 4.4).
Atosiban tidak mungkin menghambat isoform sitokrom P450 hati pada manusia (lihat bagian 4.5).
05.3 Data keamanan praklinis
Studi toksisitas, yang dilakukan pada tikus dan anjing, diberikan secara intravena selama 2 minggu dosis kira-kira 10 kali lebih tinggi dari dosis terapeutik pada manusia dan selama 3 bulan, dosis hingga 20 mg / kg / hari dengan rute sc, tidak menunjukkan toksik sistemik Dosis atosiban yang lebih tinggi, yang diberikan secara subkutan, yang tidak menghasilkan reaksi merugikan sistemik, kira-kira 2 kali lebih tinggi daripada dosis terapeutik yang digunakan pada manusia.
Studi yang mengacu pada kapasitas reproduksi dan tahap awal perkembangan embrio belum dilakukan. Studi toksisitas pada kapasitas reproduksi dengan pemberian dari tahap implantasi embrio hingga tahap terakhir kehamilan tidak menunjukkan efek pada ibu atau janin. Janin tikus terkena dosis kira-kira 4 kali lebih tinggi dari yang janin manusia terkena selama infus intravena pada wanita hamil.Studi pada hewan telah menunjukkan penghambatan laktasi yang dihasilkan, seperti yang diharapkan, dari "penghambatan" aksi oksitosin.
Atosiban juga tidak menunjukkan efek onkogenik atau mutagenik dalam tes yang dilakukan in vitro adalah in vivo.
06.0 INFORMASI FARMASI
06.1 Eksipien
Manitol
asam klorida 1M
Air untuk injeksi.
06.2 Ketidakcocokan
Dengan tidak adanya studi kompatibilitas, produk obat tidak boleh dicampur dengan produk lain.
06.3 Masa berlaku
4 tahun.
Setelah botol dibuka, produk harus segera digunakan.
06.4 Tindakan pencegahan khusus untuk penyimpanan
Simpan di lemari es (2°C - 8°C).
Simpan dalam kemasan aslinya untuk melindungi dari cahaya.
06.5 Sifat kemasan langsung dan isi kemasan
Satu botol mengandung 0,9 ml larutan untuk injeksi, sesuai dengan 6,75 mg atosiban.
Botol kaca bening, borosilikat (tipe I) disegel dengan sumbat karet bromobutil silikon tipe I abu-abu dan dengan tutup flip-off logam polipropilen dan aluminium.
06.6 Petunjuk penggunaan dan penanganan
Sebelum melanjutkan dengan pemberian, periksa secara visual vial untuk keberadaan partikel asing dan ketidakjelasan larutan.
Persiapan injeksi intravena awal:
tarik 0,9 ml dari botol, berlabel 0,9 ml, larutan TRAKTOSIL 6,75 mg / 0,9 ml untuk injeksi dan berikan dosis sebagai bolus intravena lambat selama satu menit, di bawah pengawasan medis yang ketat di bangsal kebidanan.TRAKTOSIL 6,75 mg / 0,9 ml, solusi untuk injeksi, harus segera digunakan.
07.0 PEMEGANG OTORITAS PEMASARAN
Ferring Pharmaceuticals A / S
Kay Fiskers Plads 11
2300 København S
Denmark
08.0 NOMOR OTORITAS PEMASARAN
UE / 1/99/124/001
035026018
09.0 TANGGAL OTORISASI PERTAMA ATAU PEMBARUAN KUASA
Otorisasi pertama: 20.01.2000
Perpanjangan otorisasi terakhir: 20.01.2010
10.0 TANGGAL REVISI TEKS
05.08.2011