Pengertian osmosis
Osmosis adalah perjalanan spontan pelarut (yang dalam sistem biologis biasanya air), dari larutan di mana zat terlarut lebih encer ke yang lebih terkonsentrasi; gerakan ini - yang terjadi melalui membran semipermeabel - berlanjut sampai situasi kesetimbangan tercapai, di mana kedua larutan memperoleh dan mempertahankan konsentrasi yang sama.
Contoh praktis

Untuk lebih memperjelas konsep osmosis, mari kita bayangkan bahwa kita memiliki wadah yang dibagi menjadi dua kompartemen dengan volume yang sama (A dan B) oleh membran semipermeabel (yaitu, hanya permeabel untuk pelarut - dalam hal ini air - dan tidak untuk zat terlarut) kompartemen A ada larutan berair di mana satu sendok makan glukosa telah dilarutkan, sedangkan di bagian B kami memiliki larutan air dengan volume yang sama di mana tiga sendok makan glukosa telah dilarutkan (karena itu lebih pekat). perbedaan menciptakan gradien konsentrasi glukosa di sisi membran dan, karena gula ini tidak dapat melewatinya, keseimbangan tercapai dengan berlalunya air dari kompartemen A (di mana glukosa lebih encer) menuju kompartemen B (di mana glukosa lebih banyak). ). Jika Anda lebih suka, dapat juga dikatakan bahwa air melewati osmosis dari larutan yang lebih pekat (A) ke yang kurang pekat (B).
Mengikuti aliran ini, ketinggian air di B meningkat dan menurun di A, menciptakan perbedaan ketinggian tertentu di antara keduanya. Fenomena ini berakhir ketika kedua larutan mencapai konsentrasi yang sama, kemudian menjaganya tetap konstan.
Larutan hipotonik, isotonik, dan hipertonik
Mengambil dua larutan dengan konsentrasi molar yang berbeda (jumlah partikel yang terlarut berbeda di dalamnya), larutan dengan konsentrasi molar terendah didefinisikan sebagai hipotonik dan yang lebih pekat disebut hipertonik. Dua larutan malah isotonik (atau equimolar) ketika mereka memiliki konsentrasi yang sama.
Dalam contoh yang baru saja dibuat, larutan B bersifat hipertonik (oleh karena itu mengandung lebih banyak zat terlarut) daripada yang lain (didefinisikan sebagai hipotonik); oleh karena itu, dalam kondisi normal, pelarut bergerak secara osmosis dari larutan hipotonik ke hipertonik. Kami berbicara tentang kondisi standar karena, bermain dengan hukum fisika, adalah mungkin untuk membalikkan konsep osmosis dan mendukung berlalunya pelarut dari konsentrasi yang paling encer ke yang paling pekat (osmosis balik).
Tekanan osmotik dan reverse osmosis
Seperti yang dinyatakan sejauh ini, aliran bersih pelarut - yang dihasilkan oleh osmosis - berlanjut hingga kedua larutan mencapai konsentrasi yang sama. Nah, gerakan ini bisa dilawan, dihentikan, atau bahkan dibalik dengan memberikan tekanan pada kompartemen dengan konsentrasi tertinggi.

Dalam contoh sebelumnya, cukup menempatkan piston di kompartemen B (yang kita ingat memiliki konsentrasi yang lebih tinggi), dan mendorongnya ke bawah dengan kekuatan tertentu, untuk mendukung aliran air menuju A; dalam hal ini kita berbicara tentang kebalikannya. osmosa.
Tekanan osmotik adalah tekanan yang secara tepat menentang lewatnya pelarut melalui membran semipermeabel; akibatnya itu adalah tekanan yang diperlukan untuk melawan osmosis.
Untuk apa yang telah dikatakan sejauh ini, dua larutan isotonik memiliki tekanan osmotik yang sama; harus ditekankan, oleh karena itu, bahwa tekanan osmotik bergantung secara eksklusif pada jumlah partikel yang ada dalam larutan dan bukan pada sifatnya.
Osmosis dan tubuh manusia
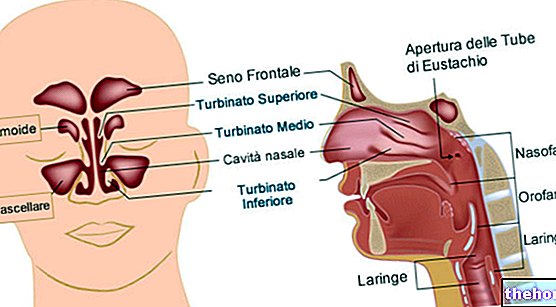
Membran plasma yang mengelilingi sel-sel tubuh manusia, pada kenyataannya, adalah membran semipermeabel, yang memungkinkan lewatnya langsung, melalui osmosis, molekul-molekul kecil (seperti air dan urea), tetapi tidak untuk molekul-molekul dengan berat molekul lebih besar ( seperti protein, asam amino dan gula). Oleh karena itu, keseimbangan osmotik dalam cairan tubuh sangat penting untuk menjamin sel-sel lingkungan yang optimal untuk hidup.
Jika kita mengambil sel seperti sel darah merah dan merendamnya dalam larutan hipotonik, ini - secara osmosis - mengalami pembengkakan (disebabkan oleh masuknya air), yang bahkan dapat membuatnya meledak. larutan hipertonik sel yang dialaminya, karena aliran air ke arah luar, dehidrasi parah yang menyebabkannya berkerut. Untungnya, dalam sel-sel organisme manusia direndam dalam larutan isotonik sehubungan dengan lingkungan internal mereka, dan ada berbagai sistem untuk menjaga cairan ini dalam keseimbangan osmotik.
Tekanan osmotik dan penyimpanan makanan
Mari kita berpikir sejenak tentang selai buatan sendiri ... gula ditambahkan dalam jumlah besar tidak hanya untuk meningkatkan rasanya, tetapi juga dan terutama untuk meningkatkan umur simpannya. Namun, gula merupakan elemen penting bagi kehidupan banyak mikroorganisme yang terlibat dalam degradasi produk. Kontradiksi yang nyata ini dibongkar oleh konsep osmosis.